دوره 28، شماره 2 - ( بهار 1401 )
جلد 28 شماره 2 صفحات 263-244 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Moradi E, Ahmadi M, Tavakoli N, Nasirzadeh F, Yoosofnejad N, Mardaneh J. Synthesis of Silver Nanoparticles of Plant Extract Pistaciaatlantica and Their Antibacterial Effects on Antibiotic Resistant Strains of S. Aureus. Intern Med Today 2022; 28 (2) :244-263
URL: http://imtj.gmu.ac.ir/article-1-3722-fa.html
URL: http://imtj.gmu.ac.ir/article-1-3722-fa.html
مرادی الهه، احمدی مبینا، توکلی نرگس، نصیرزاده فاطمه، یوسفنژاد نسترن، مردانه جلال. سنتز نانوذرات نقره گیاه بنه و اثرات ضد باکتریایی آن بر روی سویههای مقاوم به آنتیبیوتیک استافیلوکوکوس اورئوس. طب داخلی روز. 1401; 28 (2) :244-263
الهه مرادی1 
 ، مبینا احمدی2
، مبینا احمدی2 
 ، نرگس توکلی2
، نرگس توکلی2 
 ، فاطمه نصیرزاده2
، فاطمه نصیرزاده2 
 ، نسترن یوسفنژاد2
، نسترن یوسفنژاد2 
 ، جلال مردانه*
، جلال مردانه* 
 3
3

 ، مبینا احمدی2
، مبینا احمدی2 
 ، نرگس توکلی2
، نرگس توکلی2 
 ، فاطمه نصیرزاده2
، فاطمه نصیرزاده2 
 ، نسترن یوسفنژاد2
، نسترن یوسفنژاد2 
 ، جلال مردانه*
، جلال مردانه* 
 3
3
1- گروه مهندسی کشاورزی، واحد قوچان، دانشگاه آزاد اسلامی، قوچان، استان خراسان رضوی، ایران.
2- دانشآموز رشته علوم تجربی، دبیرستان شاهد ریحانهالنبی گناباد، گناباد، استان خراسان رضوی، ایران.
3- گروه میکروبشناسی، مرکز تحقیقات بیماریهای عفونی، دانشکده پزشکی، دانشگاه علومپزشکی گناباد، گناباد، استان خراسان رضوی، ایران. ، Jalalmardaneh@yahoo.com
2- دانشآموز رشته علوم تجربی، دبیرستان شاهد ریحانهالنبی گناباد، گناباد، استان خراسان رضوی، ایران.
3- گروه میکروبشناسی، مرکز تحقیقات بیماریهای عفونی، دانشکده پزشکی، دانشگاه علومپزشکی گناباد، گناباد، استان خراسان رضوی، ایران. ، Jalalmardaneh@yahoo.com
متن کامل [PDF 7098 kb]
(253 دریافت)
| چکیده (HTML) (459 مشاهده)
References
متن کامل: (172 مشاهده)
مقدمه
نانوتکنولوژی عبارت است از طراحی، شناسایی، تولید و کاربرد مواد، ابزارها و سیستمها با کنترل شکل و اندازه در مقیاس نانومتری [1]. در سالهای اخیر، همگرایی بین فناوری نانو و زیستشناسی، زمینه جدیدی از فناوری نانو ایجاد کرده است. نانوبیوتکنولوژی، علم استفاده از میکروارگانیسمها در تعدادی از فرایندهای بیوشیمیایی و بیوفیزیکی است [2]. این زمینه نسبتاً جدید بر ایجاد، راهاندازی و استفاده از مواد در مقیاس نانو در بیوتکنولوژی پیشرفته، تمرکز دارد [3].
در مقایسه با میکروارگانیسمها، استفاده از گیاهان بهدلیل نبود فرایندهای پیچیده و چندمرحلهای خاص مانند تصفیه، تهیه و نگهداری محیط کشت کارآمدتر است [4]؛ بنابراین سنتز نانوذرات توسط گیاهان سریعتر، ارزانتر و در مقیاس بزرگتر از میکروارگانیسمها است [5, 6]. توجه به تولید نانوذرات سبز باعث شروع مطالعه جامعی شده است که نشان میدهد استفاده از عصارههای گیاهی، مؤثرترین راه برای تولید نانوذرات دوستدار محیطزیست است [7, 8].
عصاره گیاه حاوی مواد فعالی است که مسئول کاهش یونهای فلزی نانوذرات سنتز است [9]. از مزایای استفاده از گیاهان در سنتز نانوذرات میتوان به استفاده آسان، امنیت زیستی، غیرسمی و ارزان بودن و داشتن متابولیتهای متنوعی که در کاهش یون نقش دارند، اشاره کرد [10]. بهطورکلی، خواص اصلی نانو ذرات نقره شامل سمی نبودن، پایداری بالا، آبدوستی، مقاومت حرارتی، عدم توسعه و افزایش مقاومت در میکروارگانیسمهاست [11].
مطالعات متعدد نشان دادهاند اثر ضدباکتریایی نانوذرات نقره به اندازه و شکل آنها بستگی دارد [12 ,13]. در مطالعه اسپبنوزا و همکاران، نانوذرات نقره خواص ضدباکتریایی قوی در برابر استرپتوکوک موتانس نشان دادند. نتایج این مطالعه نشان داد با کاهش اندازه نانوذرات نقره از 100 نانومتر به 16 نانومتر، حداقل غلظت بازدارندگی به نصف کاهش مییابد که بهمعنای افزایش خواص ضدباکتریایی نانوذرات نقره کوچکتر است [14].
امروزه استفاده از عصارههای گیاهی در سنتز نانوذرات فلزی، بهویژه به نقره بیشتر توجه شده است [15]. گونههای مختلفی از بنه در جهان رشد میکند. در ایران در استانهای ایلام، گیلان، آذربایجان، لرستان، کرمانشاه، همدان، کردستان، مرکزی، کرمان، فارس، تهران، خراسان و سیستانوبلوچستان میروید. عصاره استخراجشده از پسته کوهی، سبز رنگ، بسیار سبک، غلیظ و چسبنده است که مصارف دارویی فراوانی دارد و بهعنوان ملیّن قوی در درمان یبوست و اختلالات گوارشی استفاده میشود [16, 17].
همچنین شناسایی ترکیبات، فعالیت آنتیاکسیدانی و اثرات ضدباکتریایی و قارچی گیاهان دارویی اهمیت زیادی دارد [1]. با افزایش استفاده از آنتیبیوتیکهای درمانی رایج، شاهد گسترش گونههای میکروبی بیماریزای مقاوم به آنتیبیوتیک هستیم. توجه به گیاهان دارویی و بومی با اثر ضدمیکروبی، میتواند مشکلات ناشی از آنتیبیوتیکها را تا حدودی کاهش دهد. عصارهها و اسانسهای گیاهی بهعنوان یکی از عوامل ضدمیکروبی مهم در سالهای اخیر مورد توجه بسیاری از پژوهشگران در زمینههای پزشکی، دارویی و غذایی قرار گرفته است. از بین باکتریها، جنس استافیلوکوکوس از خانواده میکروکوکها بسیار مهم است. این باکتریها گرم مثبت، بیحرکت، بدون اسپور، هوازی و بیهوازی اختیاری هستند [18, 19, 20].
استافیلوکوکها بیش از 20 گونه دارند که در زیستگاههای مختلف پراکنده شدند [21]. دانشمندان با انجام آزمایشات مختلف و مصرف شیر آلوده به استافیلوکوکوس اورئوس، علائم و نشانههای مسمومیت غذایی را نشان دادند [22]. استافیلوکوکوس اورئوس نیز عامل عفونتهای بیمارستانی و عفونتهای اکتسابی از جامعه است و استافیلوکوکوس اورئوس مقاوم به آنتیبیوتیک، یکی از مشکلات جدی بیمارستان و جامعه است [23, 24].
مطالعات نشان دادهاند سنتز نانوذرات نقره سبز با استفاده از عصاره بنه کوهی کمتر شناخته شده است. بنابراین هدف از این مطالعه، سنتز نانوذرات نقره سبز از گیاه بنه کوهی در برابر باکتریهای بیماریزای گرم مثبت و غیرهوازی اختیاری استافیلوکوکوس اورئوس (1764 PTCC) مقاوم به آنتیبیوتیکها است.
مواد و روشها
مواد شیمیایی
تمام مواد شیمیایی مورد استفاده در خلوص بالا تهیه شدهاند. نیترات نقره، اسید کلریدریک و هیدروکسید سدیم از شرکت مرک آلمان تهیه شد. برای محلولسازی و شستوشو از آبمقطر 2 بار تقطیرشده (شرکت سرمسازی ثامن) استفاده شد. در این تحقیق، گیاه بنه کوهی از شهرستان بجستان در خراسانرضوی جمعآوری شد و گیاهشناس آن را تأیید کرد.
تهیه عصاره آبی گیاه بنه
برای تهیه عصاره آبی، ابتدا بنهِ باپوست با آبمقطر بهخوبی شسته شد. در دمای اتاق خشک و پوست آن جدا شد. سپس 100 گرم گیاه بنه پوستکنده، 3 بار با آبمقطر (شرکت سرمسازی ثامن) و هر بار 1 دقیقه شسته شد. سپس نمونه با الکل 70 درصد از شرکت مرک آلمان، 2 دقیقه ضدعفونی شد. درنهایت، 3 بار با آبمقطر، هر بار 2 دقیقه شستوشو شد. برای تهیه عصاره آبی ابتدا 30 گرم از گیاه مطالعهشده شسته و در دمای اتاق قرار داده شد تا کاملاً خشک شود. سپس این مقدار از بنه در ارلن 250 میلیلیتری ریخته شد و 100 میلیلیتر آب 2 بار مقطر (شرکت سرم ثامن) به آن اضافه شد. مخلوط 10 دقیقه جوشانده شد. عصاره آبی گیاه بنه با استفاده از کاغذ صافی شرکت واتمن انگلستان با منافذ 25 میکرونی فیلتر شد و برای حذف ذرات معلق در عصاره، نمونه با سانتریفیوژِ (DIGICEN21، اسپانیا) دورِ 9000 بهمدت 10 دقیقه سانتریفیوژ شد. سپس عصاره برای استفاده بعدی در یخچال (امرسان، ایران) در دمای 4 درجه سانتیگراد نگهداری شد [25].
سنتز نانو ذرات
10 میلیلیتر از عصاره بنه تهیهشده با 90 سیسی محلول 1 میلیمولار نیترات نقره مخلوط شد و محلول 24 ساعت در دمای اتاق روی همزن مغناطیسی قرار گرفت. برای مشاهده تغییرات رنگ، جذب محلول با دستگاه اسپکتروفتومتر (Uv-Vis) مدل 5700-CT ساخت تایوان در محدوده 300 تا 700 نانومتر بررسی شد. محلول حاوی نانوذرات با سرعت 12000 دور در دقیقه 15 دقیقه (DIGICEN21، اسپانیا) سانتریفیوژ شد و سپس مایع رویی دور ریخته شد [25]. رنگ محلول پس از تولید نانوذرات به قهوهای تیره تغییر میکند. این تغییر نشانه تولید نانوذرات نقره است. پس از مشاهده تغییر رنگ، نانوذرات تولیدشده زیستی برای تشخیص و شناسایی بهتر با روشهای دیگر بررسی شدند [15].
بهمنظور کاهش تعداد یونهای نقره (Ag+) و تأیید تشکیل نانوذرات نقره، پس از افزودن 1 میلیمولار محلول نیترات نقره به عصاره و مشاهده تغییر رنگ، 0/2 میلیلیتر از نمونه برداشته و با 2 میلیلیتر آبمقطر استریل مخلوط شد. جذب آن بررسی و درنهایت با طیفسنج مرئی فرابنفش در طول موجهای 300 تا 700 نانومتر خوانده شد [25].
اثرات ضدباکتریایی نانو ذرات نقره
سویه میکروبی استاندارد استافیلوکوکوس اورئوس (1764 PTCC) از مؤسسه پژوهشی علوم و صنایع غذایی ایران تهیه شد.
روش انتشار دیسک
برای تعیین خواص ضدباکتریایی عصاره آبی گیاه بنه، باکتری لیوفیلیزه استافیلوکوکوس اورئوس با کد 1764 PTCC ابتدا روی مولر هینتون براث شرکت مرک آلمان تلقیح و کشت میکروبی 24 ساعت در انکوباتور در دمای 37 درجه سانتیگراد انکوبه شد. از سوسپانسیون فوق پس از ورتکس برای تهیه مکفارلند 0/5 استفاده شد. بدینترتیب، سوسپانسیون در لایههای مخصوص اسپکتروفتومتر ریخته و میزان جذب نور آنها مشخص شد. برای ایجاد کدورت 0/5 مک فالن، جذب نور در طول موج 620 نانومتر باید 0/08-0/1 باشد که معادل واحد کلنی در هر میلیلیتر از باکتری است. سپس 100 میکرولیتر سوسپانسیون میکروبی روی پلیت حاوی محیط کشت مولر هینتون آگار پخش و در مرحله بعد، دیسک عصاره با غلظت 1000 میکروگرم بر میلیلیتر در پلیت حاوی محیط کشت قرار داده شد. از دیسک حاوی آنتیبیوتیک جنتامایسین (10 میکروگرم) ساخت شرکت پادتن طب بهعنوان کنترل مثبت و دیسک حاوی محلول آبمقطر دیونیزه بهعنوان کنترل منفی استفاده شد. پلیتها 24 ساعت در دمای 37 درجه سانتیگراد نگهداری شدند. قطر ناحیه بازدارنده رشد با کولیس برحسب میلیمتر اندازهگیری و میانگین آن ثبت شد [26].
تعیین حداقل غلظت بازدارندگی با روش میکرودایلوشن
در این مطالعه، از روش میکرودایلوشن براث برای تعیین حداقل غلظت مهاری استفاده شد. حداقل غلظتی که در آن عصاره از رشد میکروارگانیسم آزمایششده جلوگیری میکند (غلظت آخرین چاهی که در آن کدورت ایجاد نشده است). بدینترتیب، سویه باکتریایی استافیلوکوکوس اورئوس در محیط کشت مولرهینتون با کدورت 0/5 مکفارلند معادل واحد کلنی (در هر میلیلیتر) تهیه شد و پس از رقیقسازی، سوسپانسیونی با غلظت واحد کلنی (در هر میلیلیتر) به دست آمد.
همچنین از عصاره آبی گیاه بنه با غلظت 100 میکروگرم بر میلیلیتر، رقتهای متوالی در آبگوشت تهیه و 100 میکرولیتر از رقتهای مختلف عصاره در میکروپلیت 96 خانه ریخته شد. سپس 95 میکرولیتر محیط کشت براث و 5 میکرولیتر سوسپانسیون باکتریایی اضافه شد. این آزمایش در 3 تکرار انجام شد. همچنین چاههای حاوی 200 میکرولیتر محیط کشت براث با باکتری بهعنوان شاهد مثبت و یک چاه حاوی محیط کشت، باکتری و آنتیبیوتیک (جنتامایسین) بهعنوان شاهد منفی درنظر گرفته شدند. سپس میکروپلیتها جوشانده و در دمای 37 درجه سانتیگراد 24 ساعت انکوبه شدند. پس از 24 ساعت کدورت در طول موج 630 نانومتر به کمک کرومات مدل 4300 ELIZARIDER ساخت ایالات متحده آمریکا خوانده شد. نتایج ثبت و سپس حداقل غلظت بازدارندگی از روی آن محاسبه شد (تصویر شماره 1) [27, 28].
نانوتکنولوژی عبارت است از طراحی، شناسایی، تولید و کاربرد مواد، ابزارها و سیستمها با کنترل شکل و اندازه در مقیاس نانومتری [1]. در سالهای اخیر، همگرایی بین فناوری نانو و زیستشناسی، زمینه جدیدی از فناوری نانو ایجاد کرده است. نانوبیوتکنولوژی، علم استفاده از میکروارگانیسمها در تعدادی از فرایندهای بیوشیمیایی و بیوفیزیکی است [2]. این زمینه نسبتاً جدید بر ایجاد، راهاندازی و استفاده از مواد در مقیاس نانو در بیوتکنولوژی پیشرفته، تمرکز دارد [3].
در مقایسه با میکروارگانیسمها، استفاده از گیاهان بهدلیل نبود فرایندهای پیچیده و چندمرحلهای خاص مانند تصفیه، تهیه و نگهداری محیط کشت کارآمدتر است [4]؛ بنابراین سنتز نانوذرات توسط گیاهان سریعتر، ارزانتر و در مقیاس بزرگتر از میکروارگانیسمها است [5, 6]. توجه به تولید نانوذرات سبز باعث شروع مطالعه جامعی شده است که نشان میدهد استفاده از عصارههای گیاهی، مؤثرترین راه برای تولید نانوذرات دوستدار محیطزیست است [7, 8].
عصاره گیاه حاوی مواد فعالی است که مسئول کاهش یونهای فلزی نانوذرات سنتز است [9]. از مزایای استفاده از گیاهان در سنتز نانوذرات میتوان به استفاده آسان، امنیت زیستی، غیرسمی و ارزان بودن و داشتن متابولیتهای متنوعی که در کاهش یون نقش دارند، اشاره کرد [10]. بهطورکلی، خواص اصلی نانو ذرات نقره شامل سمی نبودن، پایداری بالا، آبدوستی، مقاومت حرارتی، عدم توسعه و افزایش مقاومت در میکروارگانیسمهاست [11].
مطالعات متعدد نشان دادهاند اثر ضدباکتریایی نانوذرات نقره به اندازه و شکل آنها بستگی دارد [12 ,13]. در مطالعه اسپبنوزا و همکاران، نانوذرات نقره خواص ضدباکتریایی قوی در برابر استرپتوکوک موتانس نشان دادند. نتایج این مطالعه نشان داد با کاهش اندازه نانوذرات نقره از 100 نانومتر به 16 نانومتر، حداقل غلظت بازدارندگی به نصف کاهش مییابد که بهمعنای افزایش خواص ضدباکتریایی نانوذرات نقره کوچکتر است [14].
امروزه استفاده از عصارههای گیاهی در سنتز نانوذرات فلزی، بهویژه به نقره بیشتر توجه شده است [15]. گونههای مختلفی از بنه در جهان رشد میکند. در ایران در استانهای ایلام، گیلان، آذربایجان، لرستان، کرمانشاه، همدان، کردستان، مرکزی، کرمان، فارس، تهران، خراسان و سیستانوبلوچستان میروید. عصاره استخراجشده از پسته کوهی، سبز رنگ، بسیار سبک، غلیظ و چسبنده است که مصارف دارویی فراوانی دارد و بهعنوان ملیّن قوی در درمان یبوست و اختلالات گوارشی استفاده میشود [16, 17].
همچنین شناسایی ترکیبات، فعالیت آنتیاکسیدانی و اثرات ضدباکتریایی و قارچی گیاهان دارویی اهمیت زیادی دارد [1]. با افزایش استفاده از آنتیبیوتیکهای درمانی رایج، شاهد گسترش گونههای میکروبی بیماریزای مقاوم به آنتیبیوتیک هستیم. توجه به گیاهان دارویی و بومی با اثر ضدمیکروبی، میتواند مشکلات ناشی از آنتیبیوتیکها را تا حدودی کاهش دهد. عصارهها و اسانسهای گیاهی بهعنوان یکی از عوامل ضدمیکروبی مهم در سالهای اخیر مورد توجه بسیاری از پژوهشگران در زمینههای پزشکی، دارویی و غذایی قرار گرفته است. از بین باکتریها، جنس استافیلوکوکوس از خانواده میکروکوکها بسیار مهم است. این باکتریها گرم مثبت، بیحرکت، بدون اسپور، هوازی و بیهوازی اختیاری هستند [18, 19, 20].
استافیلوکوکها بیش از 20 گونه دارند که در زیستگاههای مختلف پراکنده شدند [21]. دانشمندان با انجام آزمایشات مختلف و مصرف شیر آلوده به استافیلوکوکوس اورئوس، علائم و نشانههای مسمومیت غذایی را نشان دادند [22]. استافیلوکوکوس اورئوس نیز عامل عفونتهای بیمارستانی و عفونتهای اکتسابی از جامعه است و استافیلوکوکوس اورئوس مقاوم به آنتیبیوتیک، یکی از مشکلات جدی بیمارستان و جامعه است [23, 24].
مطالعات نشان دادهاند سنتز نانوذرات نقره سبز با استفاده از عصاره بنه کوهی کمتر شناخته شده است. بنابراین هدف از این مطالعه، سنتز نانوذرات نقره سبز از گیاه بنه کوهی در برابر باکتریهای بیماریزای گرم مثبت و غیرهوازی اختیاری استافیلوکوکوس اورئوس (1764 PTCC) مقاوم به آنتیبیوتیکها است.
مواد و روشها
مواد شیمیایی
تمام مواد شیمیایی مورد استفاده در خلوص بالا تهیه شدهاند. نیترات نقره، اسید کلریدریک و هیدروکسید سدیم از شرکت مرک آلمان تهیه شد. برای محلولسازی و شستوشو از آبمقطر 2 بار تقطیرشده (شرکت سرمسازی ثامن) استفاده شد. در این تحقیق، گیاه بنه کوهی از شهرستان بجستان در خراسانرضوی جمعآوری شد و گیاهشناس آن را تأیید کرد.
تهیه عصاره آبی گیاه بنه
برای تهیه عصاره آبی، ابتدا بنهِ باپوست با آبمقطر بهخوبی شسته شد. در دمای اتاق خشک و پوست آن جدا شد. سپس 100 گرم گیاه بنه پوستکنده، 3 بار با آبمقطر (شرکت سرمسازی ثامن) و هر بار 1 دقیقه شسته شد. سپس نمونه با الکل 70 درصد از شرکت مرک آلمان، 2 دقیقه ضدعفونی شد. درنهایت، 3 بار با آبمقطر، هر بار 2 دقیقه شستوشو شد. برای تهیه عصاره آبی ابتدا 30 گرم از گیاه مطالعهشده شسته و در دمای اتاق قرار داده شد تا کاملاً خشک شود. سپس این مقدار از بنه در ارلن 250 میلیلیتری ریخته شد و 100 میلیلیتر آب 2 بار مقطر (شرکت سرم ثامن) به آن اضافه شد. مخلوط 10 دقیقه جوشانده شد. عصاره آبی گیاه بنه با استفاده از کاغذ صافی شرکت واتمن انگلستان با منافذ 25 میکرونی فیلتر شد و برای حذف ذرات معلق در عصاره، نمونه با سانتریفیوژِ (DIGICEN21، اسپانیا) دورِ 9000 بهمدت 10 دقیقه سانتریفیوژ شد. سپس عصاره برای استفاده بعدی در یخچال (امرسان، ایران) در دمای 4 درجه سانتیگراد نگهداری شد [25].
سنتز نانو ذرات
10 میلیلیتر از عصاره بنه تهیهشده با 90 سیسی محلول 1 میلیمولار نیترات نقره مخلوط شد و محلول 24 ساعت در دمای اتاق روی همزن مغناطیسی قرار گرفت. برای مشاهده تغییرات رنگ، جذب محلول با دستگاه اسپکتروفتومتر (Uv-Vis) مدل 5700-CT ساخت تایوان در محدوده 300 تا 700 نانومتر بررسی شد. محلول حاوی نانوذرات با سرعت 12000 دور در دقیقه 15 دقیقه (DIGICEN21، اسپانیا) سانتریفیوژ شد و سپس مایع رویی دور ریخته شد [25]. رنگ محلول پس از تولید نانوذرات به قهوهای تیره تغییر میکند. این تغییر نشانه تولید نانوذرات نقره است. پس از مشاهده تغییر رنگ، نانوذرات تولیدشده زیستی برای تشخیص و شناسایی بهتر با روشهای دیگر بررسی شدند [15].
بهمنظور کاهش تعداد یونهای نقره (Ag+) و تأیید تشکیل نانوذرات نقره، پس از افزودن 1 میلیمولار محلول نیترات نقره به عصاره و مشاهده تغییر رنگ، 0/2 میلیلیتر از نمونه برداشته و با 2 میلیلیتر آبمقطر استریل مخلوط شد. جذب آن بررسی و درنهایت با طیفسنج مرئی فرابنفش در طول موجهای 300 تا 700 نانومتر خوانده شد [25].
اثرات ضدباکتریایی نانو ذرات نقره
سویه میکروبی استاندارد استافیلوکوکوس اورئوس (1764 PTCC) از مؤسسه پژوهشی علوم و صنایع غذایی ایران تهیه شد.
روش انتشار دیسک
برای تعیین خواص ضدباکتریایی عصاره آبی گیاه بنه، باکتری لیوفیلیزه استافیلوکوکوس اورئوس با کد 1764 PTCC ابتدا روی مولر هینتون براث شرکت مرک آلمان تلقیح و کشت میکروبی 24 ساعت در انکوباتور در دمای 37 درجه سانتیگراد انکوبه شد. از سوسپانسیون فوق پس از ورتکس برای تهیه مکفارلند 0/5 استفاده شد. بدینترتیب، سوسپانسیون در لایههای مخصوص اسپکتروفتومتر ریخته و میزان جذب نور آنها مشخص شد. برای ایجاد کدورت 0/5 مک فالن، جذب نور در طول موج 620 نانومتر باید 0/08-0/1 باشد که معادل واحد کلنی در هر میلیلیتر از باکتری است. سپس 100 میکرولیتر سوسپانسیون میکروبی روی پلیت حاوی محیط کشت مولر هینتون آگار پخش و در مرحله بعد، دیسک عصاره با غلظت 1000 میکروگرم بر میلیلیتر در پلیت حاوی محیط کشت قرار داده شد. از دیسک حاوی آنتیبیوتیک جنتامایسین (10 میکروگرم) ساخت شرکت پادتن طب بهعنوان کنترل مثبت و دیسک حاوی محلول آبمقطر دیونیزه بهعنوان کنترل منفی استفاده شد. پلیتها 24 ساعت در دمای 37 درجه سانتیگراد نگهداری شدند. قطر ناحیه بازدارنده رشد با کولیس برحسب میلیمتر اندازهگیری و میانگین آن ثبت شد [26].
تعیین حداقل غلظت بازدارندگی با روش میکرودایلوشن
در این مطالعه، از روش میکرودایلوشن براث برای تعیین حداقل غلظت مهاری استفاده شد. حداقل غلظتی که در آن عصاره از رشد میکروارگانیسم آزمایششده جلوگیری میکند (غلظت آخرین چاهی که در آن کدورت ایجاد نشده است). بدینترتیب، سویه باکتریایی استافیلوکوکوس اورئوس در محیط کشت مولرهینتون با کدورت 0/5 مکفارلند معادل واحد کلنی (در هر میلیلیتر) تهیه شد و پس از رقیقسازی، سوسپانسیونی با غلظت واحد کلنی (در هر میلیلیتر) به دست آمد.
همچنین از عصاره آبی گیاه بنه با غلظت 100 میکروگرم بر میلیلیتر، رقتهای متوالی در آبگوشت تهیه و 100 میکرولیتر از رقتهای مختلف عصاره در میکروپلیت 96 خانه ریخته شد. سپس 95 میکرولیتر محیط کشت براث و 5 میکرولیتر سوسپانسیون باکتریایی اضافه شد. این آزمایش در 3 تکرار انجام شد. همچنین چاههای حاوی 200 میکرولیتر محیط کشت براث با باکتری بهعنوان شاهد مثبت و یک چاه حاوی محیط کشت، باکتری و آنتیبیوتیک (جنتامایسین) بهعنوان شاهد منفی درنظر گرفته شدند. سپس میکروپلیتها جوشانده و در دمای 37 درجه سانتیگراد 24 ساعت انکوبه شدند. پس از 24 ساعت کدورت در طول موج 630 نانومتر به کمک کرومات مدل 4300 ELIZARIDER ساخت ایالات متحده آمریکا خوانده شد. نتایج ثبت و سپس حداقل غلظت بازدارندگی از روی آن محاسبه شد (تصویر شماره 1) [27, 28].
تعیین حداقل غلظت باکتریکشی
پس از تعیین حداقل غلظت بازدارندگی، آزمایش تعیین حداقل غلظت باکتریکش انجام شد. برای این منظور و در جهت تعیین حداقل غلظت کشنده عصاره در برابر باکتریها، از لولههای شفافی که در آنها از رشد جلوگیری شده بود، برای کشت استفاده شد و 50 میکرولیتر چاهک برداشته شد و در پلیتهای حاوی محیط کشت جامد مولر هینتون کشت داده شد. این صفحات 72 ساعت در دمای 37 درجه سانتیگراد انکوبه شدند. پس از آن، رشد نکردن باکتری حداقل غلظت کشنده عصاره را نشان داد [29].
تعیین اندازه و مورفولوژی نانو ذرات
در این مطالعه، میانگین اندازه و توزیع اندازه نانوذرات نقره سنتزشده با استفاده از ZS eutacizerDYNAMIC Light Scattering ،(England Malvern) بهعنوان مدل 3600 Zen تعیین شد. در این مرحله، عدد شاخص پراکندگی تعیین میشود که نشاندهنده میزان همگنی اندازه نانوذرات در محلول است [30].
یافتهها
سنتز نانو ذرات
روش سنتز سبز نانوذرات نقره با استفاده از احیای یونهای نقره با عصاره بنه انجام شد. اولین نشانه تولید نانوذرات نقره، تغییر رنگ محلول است. عصاره آبی گیاه بنه، سفیدرنگ بود. پس از 2/5 ساعت افزودن محلول نیترات نقره و قرار گرفتن در دمای محیط، شروع به تغییر رنگ کرد که نشاندهنده سرعت واکنش بیشتری است. بعد از 22 ساعت، رنگ قهوهای تیره نشاندهنده تولید نانوذرات نقره در محلول است که با منابع مطابقت داشت. ظهور رنگ قهوهای تیره پس از واکنش با یونهای نقره، نشانگر بارز کاهش یونهای فلزی و تشکیل نانوذرات نقره در محیط است (تصویر شماره 2) [10].
پس از تعیین حداقل غلظت بازدارندگی، آزمایش تعیین حداقل غلظت باکتریکش انجام شد. برای این منظور و در جهت تعیین حداقل غلظت کشنده عصاره در برابر باکتریها، از لولههای شفافی که در آنها از رشد جلوگیری شده بود، برای کشت استفاده شد و 50 میکرولیتر چاهک برداشته شد و در پلیتهای حاوی محیط کشت جامد مولر هینتون کشت داده شد. این صفحات 72 ساعت در دمای 37 درجه سانتیگراد انکوبه شدند. پس از آن، رشد نکردن باکتری حداقل غلظت کشنده عصاره را نشان داد [29].
تعیین اندازه و مورفولوژی نانو ذرات
در این مطالعه، میانگین اندازه و توزیع اندازه نانوذرات نقره سنتزشده با استفاده از ZS eutacizerDYNAMIC Light Scattering ،(England Malvern) بهعنوان مدل 3600 Zen تعیین شد. در این مرحله، عدد شاخص پراکندگی تعیین میشود که نشاندهنده میزان همگنی اندازه نانوذرات در محلول است [30].
یافتهها
سنتز نانو ذرات
روش سنتز سبز نانوذرات نقره با استفاده از احیای یونهای نقره با عصاره بنه انجام شد. اولین نشانه تولید نانوذرات نقره، تغییر رنگ محلول است. عصاره آبی گیاه بنه، سفیدرنگ بود. پس از 2/5 ساعت افزودن محلول نیترات نقره و قرار گرفتن در دمای محیط، شروع به تغییر رنگ کرد که نشاندهنده سرعت واکنش بیشتری است. بعد از 22 ساعت، رنگ قهوهای تیره نشاندهنده تولید نانوذرات نقره در محلول است که با منابع مطابقت داشت. ظهور رنگ قهوهای تیره پس از واکنش با یونهای نقره، نشانگر بارز کاهش یونهای فلزی و تشکیل نانوذرات نقره در محیط است (تصویر شماره 2) [10].
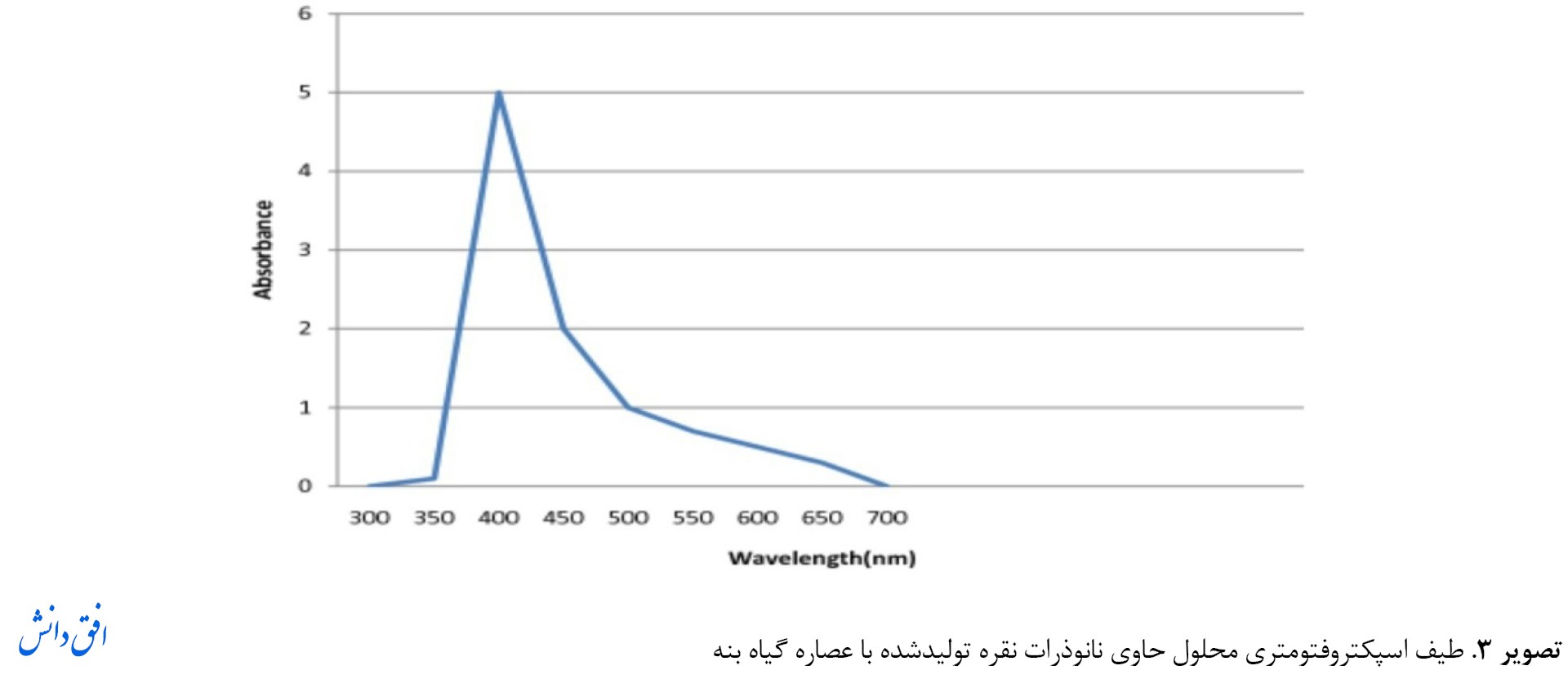
زمانی که تغییر رنگ با تشکیل رسوب همراه باشد، نانوذرات تشکیلشده از نظر اندازه ذرات بزرگ هستند و وقتی تغییر رنگ دادند، رسوب تشکیل نمیشود، نانوذرات سنتزشده تا حدی بسیار کوچک هستند و در بهترین حالت خود قرار دارند. در هیچیک از محلولهای نانوذراتی تولیدشده با عصاره بنه، رسوب تشکیل نشد که نشاندهنده اندازه ذرات مناسب نانوذرات بنه است. نتایج طیفسنجی مرئی فرابنفش عصاره بنه پس از سنتز نانوذرات نقره نشان داد حداکثر پیک جذب منحنی در محدوده 350 تا 450 نانومتر است که نشاندهنده سنتز نانوذرات نقره است (تصویر شماره 3) [10].
نتایج آزمونهای میکروبی نانو ذرات نقره
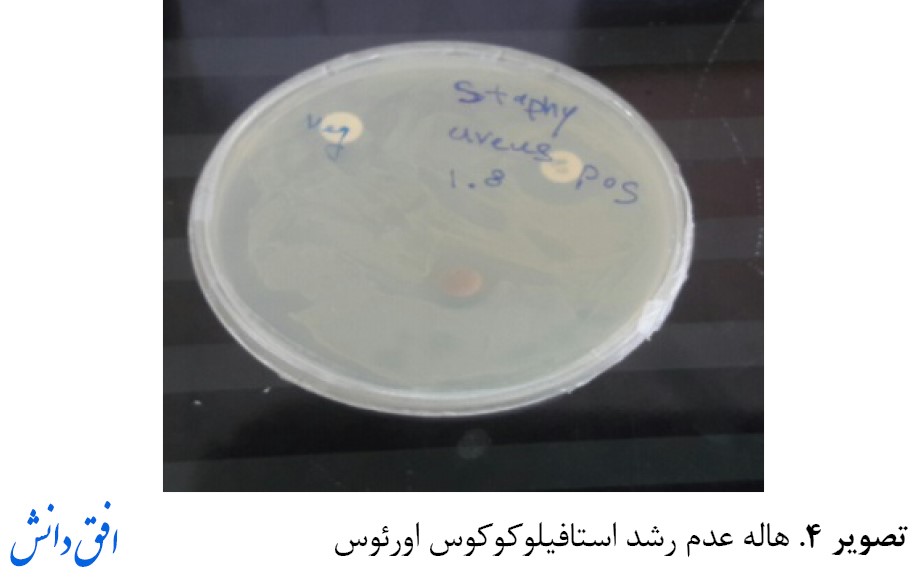
نتایج دیفیوژن دیسک (قطر هاله عدم رشد) با کولیس برحسب میلیمتر اندازهگیری و میانگین ثبت شد. همانطور که در نتایج مشاهده میشود، قطر ناحیه بازدارنده رشد استافیلوکوکوس اورئوس در اطراف دیسک آنتیبیوتیک جنتامایسین 17 میلیمتر و قطر ناحیه بازدارنده رشد استافیلوکوکوس اورئوس در اطراف دیسک با عصاره آبی نانوذرات بنه با غلظت آغشته شده است. از 1000 میکروگرم/میلیلیتر، 12 میلیمتر مشاهده شد. این بدان معناست که عصاره آبی نانوذرات بنه میتواند بهخوبی از رشد استافیلوکوکوس اورئوس جلوگیری کند (تصویر شماره 4 و جدول شماره 1).

نتایج دیفیوژن دیسک (قطر هاله عدم رشد) با کولیس برحسب میلیمتر اندازهگیری و میانگین ثبت شد. همانطور که در نتایج مشاهده میشود، قطر ناحیه بازدارنده رشد استافیلوکوکوس اورئوس در اطراف دیسک آنتیبیوتیک جنتامایسین 17 میلیمتر و قطر ناحیه بازدارنده رشد استافیلوکوکوس اورئوس در اطراف دیسک با عصاره آبی نانوذرات بنه با غلظت آغشته شده است. از 1000 میکروگرم/میلیلیتر، 12 میلیمتر مشاهده شد. این بدان معناست که عصاره آبی نانوذرات بنه میتواند بهخوبی از رشد استافیلوکوکوس اورئوس جلوگیری کند (تصویر شماره 4 و جدول شماره 1).

حداقل غلظت بازدارندگی و حداقل غلظت باکتریکشی نانوذرات و عصاره بنه روی استافیلوکوکوس اورئوس تعیین شد. همانطور که در جدول شماره 1 مشاهده میشود، در این مطالعه کمترین نانوذرات و عصارههای بازدارنده برای استافیلوکوک 12/5 میکروگرم بر میلیلیتر و کمترین غلظت باکتریکشی نانوذرات و عصارهها، 12/5 میکروگرم بر میلیلیتر تعیین شد (تصویر شماره 5).
نتایج تجزیهوتحلیل پراکندگی نور دینامیکی
پراکندگی نور دینامیکی، روش فیزیکی سریع و غیرمخربی است که برای تعیین توزیع اندازه ذرات در محلول و سوسپانسیون و برای مطالعه رفتار انتشار ماکرومولکولها در محلول استفاده میشود. در این مطالعه از این آزمون برای تعیین پارامترهای زیر استفاده شد:
اندازهگیری قطر هیدرودینامیکی ذرات در حالت تعلیق (Z-Average)
نتایج آزمون پراکندگی نور دینامیکی میتواند بهعنوان روش مکملی برای مطالعات تحلیلی و بهعنوان ابزاری برای مطالعه مدلهای پراکندگی با استفاده از شعاع هیدرودینامیکی استفاده شود. قطر بهدستآمده با این روش مربوط به کرهای با ضریب انتقال معادل ذره اندازهگیری شده است.
ضریب انتقال بهاندازه ذرات، ساختار سطح، غلظت و نوع یونهای موجود در محیط بستگی دارد، به این معنا که اندازه بهدستآمده با این روش میتواند بزرگتر از مقدار بهدستآمده با میکروسکوپ الکترونی باشد. ضریب انتشار یا ضریب انتشار وابسته به غلظت است و باید در غلظتهای مختلف اندازهگیری شود و بهعنوان یک عملیات استاندارد به رقت بینهایت برسد. در تعیین سایر پارامترهای هیدرودینامیکی مهم و بسیار مفید است. برای مثال، شعاع هیدرودینامیکی را میتوان با فرمول معروف استوکس-انیشتین (فرمول شماره 1) به دست آورد.
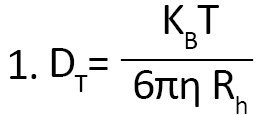
Rh شعاع هیدرودینامیکی ذره، KB،ثابت بولتزمن، η ویسکوزیته حلّال است که به دما وابسته بوده و به چگالی و فشار سیستم مرتبط نیست، T دمای مطلق و ضریب نفوذ است [31].
تعیین توزیع اندازه ذرات با استفاده از شاخص بدون بُعد (PDI)
اگر مقدار PDI کمتر از 0/05 باشد، ذرات توزیع یکنواخت عالی دارند. اگر مقدار PDI بزرگتر از 0/7 باشد، نشاندهنده این است که نمونه توزیع، اندازه بسیار گستردهای دارد و احتمالاً برای روش پراکندگی نور دینامیکی مناسب نیست و بهطورکلی اگر اندازه این شاخص بین 0/1 تا 0/5 باشد، ذرات توزیع یکنواخت خوبی دارد. اندازه قطر هیدرودینامیکی و عدد PDI نمونه در جدول شماره 2 ارائه شده است.

همانطور که نتیجه پراکندگی نور دینامیکی نشان میدهد، قطر هیدرودینامیکی نانوذرات 1132 نانومتر است. مقدار PDI، 0/373 است که نشان میدهد نانوذرات در حالت پایدار هستند (PDI>0/7>0/1) و توزیع اندازه ذرات مناسب است (جدول شماره 3).

اندازهگیری دقیق سایز نانوذرات با زتاسایزر
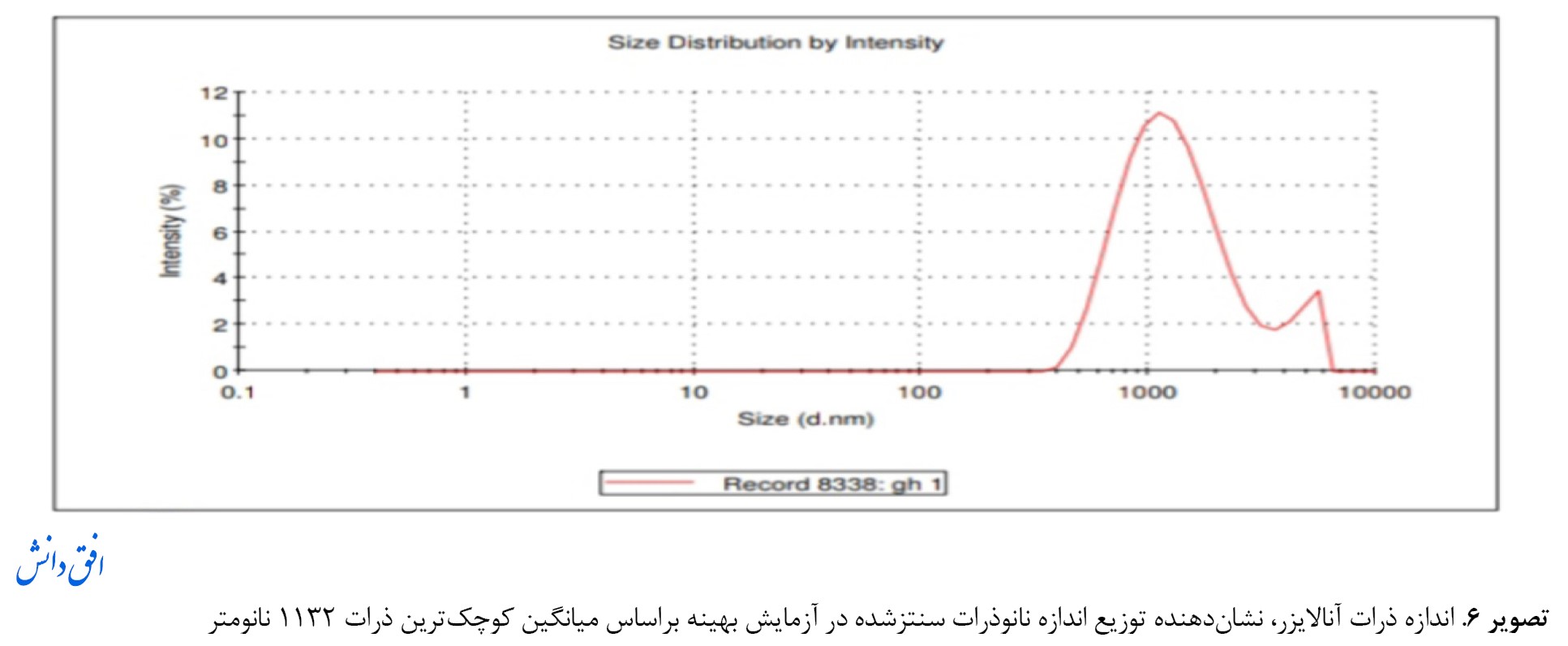
نتایج تحلیلگر اندازه ذرات نشان داد اندازه نانوذرات سنتزشده 1132 نانومتر است. تصویر شماره 6، دو قله 1132 نانومتر و 4707 نانومتر را نشان میدهد.
پراکندگی نور دینامیکی، روش فیزیکی سریع و غیرمخربی است که برای تعیین توزیع اندازه ذرات در محلول و سوسپانسیون و برای مطالعه رفتار انتشار ماکرومولکولها در محلول استفاده میشود. در این مطالعه از این آزمون برای تعیین پارامترهای زیر استفاده شد:
اندازهگیری قطر هیدرودینامیکی ذرات در حالت تعلیق (Z-Average)
نتایج آزمون پراکندگی نور دینامیکی میتواند بهعنوان روش مکملی برای مطالعات تحلیلی و بهعنوان ابزاری برای مطالعه مدلهای پراکندگی با استفاده از شعاع هیدرودینامیکی استفاده شود. قطر بهدستآمده با این روش مربوط به کرهای با ضریب انتقال معادل ذره اندازهگیری شده است.
ضریب انتقال بهاندازه ذرات، ساختار سطح، غلظت و نوع یونهای موجود در محیط بستگی دارد، به این معنا که اندازه بهدستآمده با این روش میتواند بزرگتر از مقدار بهدستآمده با میکروسکوپ الکترونی باشد. ضریب انتشار یا ضریب انتشار وابسته به غلظت است و باید در غلظتهای مختلف اندازهگیری شود و بهعنوان یک عملیات استاندارد به رقت بینهایت برسد. در تعیین سایر پارامترهای هیدرودینامیکی مهم و بسیار مفید است. برای مثال، شعاع هیدرودینامیکی را میتوان با فرمول معروف استوکس-انیشتین (فرمول شماره 1) به دست آورد.
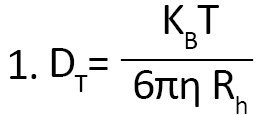
Rh شعاع هیدرودینامیکی ذره، KB،ثابت بولتزمن، η ویسکوزیته حلّال است که به دما وابسته بوده و به چگالی و فشار سیستم مرتبط نیست، T دمای مطلق و ضریب نفوذ است [31].
تعیین توزیع اندازه ذرات با استفاده از شاخص بدون بُعد (PDI)
اگر مقدار PDI کمتر از 0/05 باشد، ذرات توزیع یکنواخت عالی دارند. اگر مقدار PDI بزرگتر از 0/7 باشد، نشاندهنده این است که نمونه توزیع، اندازه بسیار گستردهای دارد و احتمالاً برای روش پراکندگی نور دینامیکی مناسب نیست و بهطورکلی اگر اندازه این شاخص بین 0/1 تا 0/5 باشد، ذرات توزیع یکنواخت خوبی دارد. اندازه قطر هیدرودینامیکی و عدد PDI نمونه در جدول شماره 2 ارائه شده است.

همانطور که نتیجه پراکندگی نور دینامیکی نشان میدهد، قطر هیدرودینامیکی نانوذرات 1132 نانومتر است. مقدار PDI، 0/373 است که نشان میدهد نانوذرات در حالت پایدار هستند (PDI>0/7>0/1) و توزیع اندازه ذرات مناسب است (جدول شماره 3).

اندازهگیری دقیق سایز نانوذرات با زتاسایزر
نتایج تحلیلگر اندازه ذرات نشان داد اندازه نانوذرات سنتزشده 1132 نانومتر است. تصویر شماره 6، دو قله 1132 نانومتر و 4707 نانومتر را نشان میدهد.
بحث
فناوری نانو نقره در مواد ضدباکتریایی انقلابی ایجاد کرده که کانون اصلی توسعه محصولات نانونقره است و نسبت به مواد شیمیایی مزایای زیادی دارد [33]. یکی از معایب روشهای شیمیایی برای تولید نانوذرات، سرعت پایین تولید و انرژیهای بالا طی فرایند واکنش است [34]، اما در روش سنتز سبز، استفاده از ترکیبات گیاهی بدون نیاز به سورفکتانت، شرایط خاص و سایر عوامل تثبیتکننده انجام میشود [35]. بنابراین در این تحقیق، نانوذرات نقره با استفاده از عصاره آبی گیاه بنه به روش زیستپالایی تولید و اثرات ضدباکتریایی آن بررسی شد. اساس سنتز نانوذرات کاهش یونهای نمک آنها و درواقع، خنثیسازی بار الکتریکی است. در این تحقیق، این فرایند 22 ساعت در دمای اتاق تکمیل شد که نشاندهنده سرعت بالای این روش و نیاز آن به دماهای بالا برای تشکیل نانوذرات نقره است که مشابه نتایج تحقیقات سیورامان و همکاران و ساتیاوات و همکاران است [36, 37].
عصاره بنه با فلاونوئیدها، آلکالوئیدها، تریترپنوئیدها و ساپونینهای بالا، پتانسیل بالایی برای کاهش نانوذرات نقره دارد [38]. اکسیداسیون گروههای عاملی مانند هیدروکسیل، کربونیل، آلدئید میتواند یونهای نقره را کاهش دهد و درنتیجه، نانوذرات نقره تولید شود [39, 40].
در تصویر شماره 2، تغییر رنگ مشاهدهشده به قهوهای تیره در عصاره بنه از تشکیل نانوذرات نقره فعال، نشانه واضحی بود [41] و همچنین نتایج کاملاً مشابه نتایج تحقیقات ردی و گاندی [42] بود.
همانطور که در تصویر شماره 3 نشان داده شد، پیک تشکیلشده در طول موج 400 تا 450 نانومتر نشاندهنده تشکیل نانوذرات نقره است و مربوط به رزونانس پلاسمون سطحی نانوذرات نقره است که به القای الکترونهای آزاد در نانوذرات نسبت داده میشود [43]. اندازه قطرهای هیدرودینامیکی (Z-Average) و توزیع اندازه ذرات (PDI) با روش پراکندگی نور دینامیکی اندازهگیری شد. نتایج نشان داد اندازه نانوذرات سنتزشده با استفاده از زتاسایزر 1132 نانومتر است.
دو قله در تصویر شماره 6 دیده میشود که قله بزرگتر نشاندهنده تجمع بهدلیل بار سطحی بین ذرات است. توزیع اندازه ذرات 0/3 بود که نشان میدهد نانوذرات در حالت پایدار هستند(PDI>0/7>0/1) و توزیع اندازه ذرات مناسب است. همانطور که در منحنی توزیع اندازه ذرات نمونه در تصویر شماره 6 نشان داده شد، نبود وجود پیکهای بزرگ در نمونه شاید نشاندهنده این است که نانوذرات در محلول حجیم تشکیل نشدهاند. به این معنا که نانوذرات بهخوبی تشکیل شدهاند که با نتایج تحقیقات سایر پژوهشگران همخوانی دارد [44, 45].
درواقع، سازوکار اصلی خواص ضدباکتریایی نانوذرات نقره، آزادسازی یونهای نقره است. برخی از سازوکارهای اصلی عمل یونهای نقره عبارتاند از: آسیب به غشای سلولی، تولید گونههای فعال اکسیژن، حمله سلولی یونهای نقره (یا حتی نانوذرات نقره بهدلیل حفرههای غشایی)، آسیب بیشتر به محصولات ATP و مهار تکثیر DNA. در بسیاری از مطالعات، آسیب به غشای سلولی بهوسیله یونهای نقره گزارش شده است. این گزارشها عمدتاً براساس مشاهده حفرهها یا سوراخهای بزرگ در غشای باکتری با تجزیهوتحلیل TEM انجام میشود. یونهای نقره ممکن است با پروتئینهای غشایی حاوی گوگرد (برای مثال، تیولهای پروتئین زنجیره تنفسی) تعامل داشته باشند و باعث آسیب فیزیکی به غشا شوند [46].
وجود اثرات ضدمیکروبی قوی در محصولات گیاهی از اهمیت ویژهای برخوردار است، زیرا امروزه یکی از مشکلات عمده علم پزشکی، ایجاد مقاومت در برابر آنتیبیوتیکها در بسیاری از پاتوژنهای رایج است [47]. افزایش مقاومت آنتیبیوتیکی هزینه مراقبتهای بهداشتی را بهدلیل طول درمان (ازجمله بستری شدن در بیمارستان) و بهبود، همراه با شکست درمان آنتیبیوتیکی، نیاز به توسعه عوامل جدید آنتیبیوتیکی، استفاده از روشهای جدیتر و کنترل گستردهتر عفونت افزایش میدهد. با پیشرفت فناوری نانو و ایجاد نانوذرات نقره و خواص ضدمیکروبی اثباتشده این نانوذرات، برای جلوگیری از گسترش پاتوژنهای مقاوم به آنتیبیوتیک کاربرد دارند و استفاده از آنها در پزشکی و علوم مرتبط روزبهروز بهطور چشمگیری افزایش یافته است [48].
ترکیب این روشها با آنتیبیوتیکدرمانی میتواند انگیزه مهمی برای پژوهشگران برای مطالعه برای یافتن، خالصسازی و استانداردسازی نانو محصولات گیاهی مؤثر (که سمیت انتخابی بهتری نسبت به آنتیبیوتیکها دارند) مانند بنه باشد. تاکنون مطالعات زیادی برای بررسی خواص ضدمیکروبی عصاره صمغ بنه انجام شده است. پناهی و همکاران اثر اسانس صمغ بنه بر خواص ضدمیکروبی و آنتیاکسیدانی فیلم خوراکی نشاسته را بررسی کردند. باتوجهبه یافتههای این مطالعه، اسانس صمغ بنه را میتوان بهعنوان یک نگهدارنده طبیعی به فیلمهای زیستتخریبپذیر اضافه کرد [49].
علیزاده و همکاران، خواص فیزیکی و ضدمیکروبی فیلم خوراکی کیتوزان حاوی اسانس صمغ بنه را بررسی کردند و نتایج این مطالعه نشان داد اسانس صمغ بنه بهعنوان یک ماده ضدمیکروبی طبیعی پتانسیل بالایی برای تولید فیلمهای ضدمیکروبی دارد [50]. بااینحال، مطالعات اندکی درباره خواص ضدباکتریایی و ضدقارچی عصاره بنه بهویژه تأثیر نانوذرات تولیدشده با استفاده از عصاره این گیاه بر باکتری استافیلوکوکوس اورئوس توسط پژوهشگران گزارش شده است. بهدلیل فراوانی استافیلوکوکوس اورئوس در غذا، نقش این میکروارگانیسم را بهعنوان یکی از عوامل مسمومیت نباید نادیده گرفت.
ازآنجاکه انتروتوکسینهای این باکتری در برابر حرارت و پروتئاز مقاوم هستند و در فرایند حرارت و پخت از بین نمیروند، شیوع بالای ژنهای انتروتوکسین در این مطالعه نشاندهنده نقش بالقوه این باکتری در ایجاد مسمومیت غذایی است. افزایش شیوع و مقاومت به سایر آنتیبیوتیکها در سویههای CA.MRSA جداشده از غذا میتواند مشکلی جدی برای سلامت عمومی باشد؛ بنابراین باید برای جلوگیری از آلودگی مواد غذایی و افزایش سطح بهداشت تصمیمات جدی اتخاذ شود [51].
نتایج بررسی حداقل غلظت بازدارندگی و حداقل غلظت باکتریکشی این نوع نانوذره بر روی استافیلوکوکوس اورئوس نشان میدهد این نانوذره اثر بازدارندگی رشد و اثر کشنده بر استافیلوکوکوس اورئوس دارد. با بررسی رشد یا رشد نکردن باکتریها در محیط کشت حاوی نانوذرات، حداقل غلظت بازدارنده تعیین شد. مقایسه اثر ضدباکتریایی نانوذرات بیوسنتزشده با عصاره نشان میدهد اثر ضدباکتریایی نانوذرات بیوسنتزشده با عصاره بنه روی این باکتری بسیار مؤثر است. پیشبینی میشود خواص ضدباکتریایی خوب نانوذرات سنتزشده در این مطالعه بهدلیل وضعیت پایدار نانوذرات تشکیلشده (PDI>0/7>0/1) و توزیع اندازه مناسب نانوذرات بنه باشد [44]. در مطالعه حاضر، در نتایج بهدستآمده از آزمایش قطر متوسط هاله در غلظت 1000 میکروگرم نانوذرات بنه بر روی استافیلوکوک، قطر هاله عدم رشد 12 میلیمتر بود که بیانگر خاصیت ضدمیکروبی عصاره این گیاه است.
املیان و همکاران، سنتز نانوذرات نقره و اثرات آنتیاکسیدانی، سمیت سلولی و ضدباکتریایی آنها در شرایط آزمایشگاهی در عصاره برگ بنه را بررسی کردند و نتایج این مطالعه نشان داد نانوذرات نقره از رشد باکتریها جلوگیری میکند. غلظت 7 میکروگرم بر میلیلیتر و در غلظت 3 تا 15 میکروگرم بر میلیلیتر حذف شد. درنهایت، نانوذرات نقره سنتزشده، غیرسمیت سلولی، فعالیتهای آنتیاکسیدانی و ضدباکتریایی را به روشی وابسته به دُز نشان دادند [2].
صادقی و همکاران، سنتز سبز آسان نانوذرات نقره با استفاده از عصاره آبی گیاه بنه و فعالیت ضدباکتریایی آن را بررسی کردند. نتایج حاکی از آن بود که نانوذرات نقره سنتزشده بهعنوان عامل ضدباکتری مؤثر عمل میکنند. این مطلب که نانوذرات نقره قادر به ارائه اثر ضدباکتریایی بالا هستند و ازاینرو، پتانسیل زیادی در تهیه داروهای استفادهشده در برابر بیماریهای باکتریایی دارند، تأیید شده است.
بهطورکلی باکتریهای گرم مثبت نسبت به باکتریهای گرم منفی به عصارهها و اسانسهای گیاهی حساسیت بیشتری دارند. باتوجهبه اینکه باکتریهای گرم منفی در اطراف دیواره سلولی خود یک لایه بیرونی دارند و بهعنوان مانع عمل کرده و دسترسی ترکیبات آبگریز را محدود میکنند؛ بنابراین از حساسیت کمتری برخوردارند. یافتههای این مطالعه با نتایج سایر پژوهشگران سازگار بود [52].
باتوجهبه در دسترس بودن گیاهان مورد مطالعه در کشور ما و امکان تهیه آن با هزینه کمتر نسبت به سایر داروها و همچنین بهدلیل خواص ضدباکتریایی نانوذرات بیوسنتزشده با عصاره این گیاهان، نتایج چنین تحقیقاتی میتواند مورد توجه پژوهشگران، کارشناسان و تولیدکنندگان دارو بوده و برای مبارزه با عفونتهای ناشی از این باکتریها استفاده شود. در بین روشهای تولید نانوذرات، روش تولید سبز، ارزان، کمخطر و سازگار با محیطزیست است. نانوذرات نقره تولیدشده با این روش بهدلیل استفاده نکردن از مواد شیمیایی خطرناک، قابلیت استفاده در صنایع مرتبط با سلامت انسان را دارند. پس ترکیبی از عوامل ذکرشده باعث شد که نانوذرات نقره بهدستآمده با استفاده از عصاره این گیاه اثرات بازدارندگی خوبی بر استافیلوکوکوس اورئوس داشته باشد.
باتوجهبه مطالعات فوق میتوان نتیجه گرفت که گیاه بنه بهدلیل داشتن خواص غذایی و دارویی بالا میتواند بهعنوان گزینهای مناسب در تولید نانوذرات به روش سبز و کاربرد آن در صنایع مرتبط با سلامت انسان مانند بهداشت و درمان مواد غذایی مورد توجه قرار گیرد. نتایج این تحقیق نشان داد عصاره بنه در زمان کوتاهی قادر به کاهش یونهای نقره بهصورت نانوذرات با توزیع اندازه ذرات مناسب و پایدار است که خاصیت بازدارندگی و کشنده خوبی بر روی استافیلوکوکوس اورئوس دارد؛ بنابراین مطالعه پتانسیل عصاره بنه میتواند راهحلی برای استفاده مؤثر از آن و راهی ارزان و زیستسازگار برای تولید نانوذرات باشد.
باتوجهبه نتایج بهدستآمده در این مطالعه و اثر ضدمیکروبی خوب نانوذرات بنه بر استافیلوکوکوس اورئوس، روشهای کاهش اندازه نانوذرات نقره بنه و ارزیابی آن با سایر روشهای اندازهگیری نانوذرات و اثر ضدمیکروبی آن، توصیه میشود در مورد سایر باکتریهای گرم مثبت تحقیقات بیشتری انجام شود و از این گیاه منحصربهفرد استفاده بهینه شود.
ملاحظات اخلاقی
پیروی از اصول اخلاق پژوهش
این پژوهش، کار تحقیقاتی است که در آن ملاحظات اخلاقی وجود نداشت.
حامی مالی
این پژوهش کار گروهی جناب آقای دکتر جلال مردانه عضو گروه میکروبیولوژی، دانشکده پزشکی، مرکز تحقیقات بیماریهای عفونی، دانشگاه علوم پزشکی گناباد، الهه مرادی، دانشآموخته کارشناسی ارشد علوم و صنایع غذایی و دانشآموزان دبیرستان شاهد ریحانهالنبی شهرستان گناباد است که با حمایت مالی مدیریت محترم دبیرستان شاهد ریحانهالنبی انجام شده است.
مشارکت نویسندگان
مفهومپردازی، تحلیل دادهها و روششناسی: الهه مرادی؛ تحقیق، گردآوری اطلاعات، نگارش پیشنویس و اصلی، منابع مالی و ویرایش منابع: همه نویسندگان.
تعارض منافع
بنابر اظهار نویسندگان، این مقاله تعارض منافع ندارد.
تشکر و قدردانی
نویسندگان از مدیریت دبیرستان دخترانه ریحانهالنبی شهرستان گناباد، خانم مرادی تقدیر و تشکر میکنند. همچنین از همکاری ریاست محترم آزمایشگاه مرکزی پژوهشکده علوم و صنایع غذایی خراسان رضوی، فیضی و همکاران آنها قدردانی میشود.
فناوری نانو نقره در مواد ضدباکتریایی انقلابی ایجاد کرده که کانون اصلی توسعه محصولات نانونقره است و نسبت به مواد شیمیایی مزایای زیادی دارد [33]. یکی از معایب روشهای شیمیایی برای تولید نانوذرات، سرعت پایین تولید و انرژیهای بالا طی فرایند واکنش است [34]، اما در روش سنتز سبز، استفاده از ترکیبات گیاهی بدون نیاز به سورفکتانت، شرایط خاص و سایر عوامل تثبیتکننده انجام میشود [35]. بنابراین در این تحقیق، نانوذرات نقره با استفاده از عصاره آبی گیاه بنه به روش زیستپالایی تولید و اثرات ضدباکتریایی آن بررسی شد. اساس سنتز نانوذرات کاهش یونهای نمک آنها و درواقع، خنثیسازی بار الکتریکی است. در این تحقیق، این فرایند 22 ساعت در دمای اتاق تکمیل شد که نشاندهنده سرعت بالای این روش و نیاز آن به دماهای بالا برای تشکیل نانوذرات نقره است که مشابه نتایج تحقیقات سیورامان و همکاران و ساتیاوات و همکاران است [36, 37].
عصاره بنه با فلاونوئیدها، آلکالوئیدها، تریترپنوئیدها و ساپونینهای بالا، پتانسیل بالایی برای کاهش نانوذرات نقره دارد [38]. اکسیداسیون گروههای عاملی مانند هیدروکسیل، کربونیل، آلدئید میتواند یونهای نقره را کاهش دهد و درنتیجه، نانوذرات نقره تولید شود [39, 40].
در تصویر شماره 2، تغییر رنگ مشاهدهشده به قهوهای تیره در عصاره بنه از تشکیل نانوذرات نقره فعال، نشانه واضحی بود [41] و همچنین نتایج کاملاً مشابه نتایج تحقیقات ردی و گاندی [42] بود.
همانطور که در تصویر شماره 3 نشان داده شد، پیک تشکیلشده در طول موج 400 تا 450 نانومتر نشاندهنده تشکیل نانوذرات نقره است و مربوط به رزونانس پلاسمون سطحی نانوذرات نقره است که به القای الکترونهای آزاد در نانوذرات نسبت داده میشود [43]. اندازه قطرهای هیدرودینامیکی (Z-Average) و توزیع اندازه ذرات (PDI) با روش پراکندگی نور دینامیکی اندازهگیری شد. نتایج نشان داد اندازه نانوذرات سنتزشده با استفاده از زتاسایزر 1132 نانومتر است.
دو قله در تصویر شماره 6 دیده میشود که قله بزرگتر نشاندهنده تجمع بهدلیل بار سطحی بین ذرات است. توزیع اندازه ذرات 0/3 بود که نشان میدهد نانوذرات در حالت پایدار هستند(PDI>0/7>0/1) و توزیع اندازه ذرات مناسب است. همانطور که در منحنی توزیع اندازه ذرات نمونه در تصویر شماره 6 نشان داده شد، نبود وجود پیکهای بزرگ در نمونه شاید نشاندهنده این است که نانوذرات در محلول حجیم تشکیل نشدهاند. به این معنا که نانوذرات بهخوبی تشکیل شدهاند که با نتایج تحقیقات سایر پژوهشگران همخوانی دارد [44, 45].
درواقع، سازوکار اصلی خواص ضدباکتریایی نانوذرات نقره، آزادسازی یونهای نقره است. برخی از سازوکارهای اصلی عمل یونهای نقره عبارتاند از: آسیب به غشای سلولی، تولید گونههای فعال اکسیژن، حمله سلولی یونهای نقره (یا حتی نانوذرات نقره بهدلیل حفرههای غشایی)، آسیب بیشتر به محصولات ATP و مهار تکثیر DNA. در بسیاری از مطالعات، آسیب به غشای سلولی بهوسیله یونهای نقره گزارش شده است. این گزارشها عمدتاً براساس مشاهده حفرهها یا سوراخهای بزرگ در غشای باکتری با تجزیهوتحلیل TEM انجام میشود. یونهای نقره ممکن است با پروتئینهای غشایی حاوی گوگرد (برای مثال، تیولهای پروتئین زنجیره تنفسی) تعامل داشته باشند و باعث آسیب فیزیکی به غشا شوند [46].
وجود اثرات ضدمیکروبی قوی در محصولات گیاهی از اهمیت ویژهای برخوردار است، زیرا امروزه یکی از مشکلات عمده علم پزشکی، ایجاد مقاومت در برابر آنتیبیوتیکها در بسیاری از پاتوژنهای رایج است [47]. افزایش مقاومت آنتیبیوتیکی هزینه مراقبتهای بهداشتی را بهدلیل طول درمان (ازجمله بستری شدن در بیمارستان) و بهبود، همراه با شکست درمان آنتیبیوتیکی، نیاز به توسعه عوامل جدید آنتیبیوتیکی، استفاده از روشهای جدیتر و کنترل گستردهتر عفونت افزایش میدهد. با پیشرفت فناوری نانو و ایجاد نانوذرات نقره و خواص ضدمیکروبی اثباتشده این نانوذرات، برای جلوگیری از گسترش پاتوژنهای مقاوم به آنتیبیوتیک کاربرد دارند و استفاده از آنها در پزشکی و علوم مرتبط روزبهروز بهطور چشمگیری افزایش یافته است [48].
ترکیب این روشها با آنتیبیوتیکدرمانی میتواند انگیزه مهمی برای پژوهشگران برای مطالعه برای یافتن، خالصسازی و استانداردسازی نانو محصولات گیاهی مؤثر (که سمیت انتخابی بهتری نسبت به آنتیبیوتیکها دارند) مانند بنه باشد. تاکنون مطالعات زیادی برای بررسی خواص ضدمیکروبی عصاره صمغ بنه انجام شده است. پناهی و همکاران اثر اسانس صمغ بنه بر خواص ضدمیکروبی و آنتیاکسیدانی فیلم خوراکی نشاسته را بررسی کردند. باتوجهبه یافتههای این مطالعه، اسانس صمغ بنه را میتوان بهعنوان یک نگهدارنده طبیعی به فیلمهای زیستتخریبپذیر اضافه کرد [49].
علیزاده و همکاران، خواص فیزیکی و ضدمیکروبی فیلم خوراکی کیتوزان حاوی اسانس صمغ بنه را بررسی کردند و نتایج این مطالعه نشان داد اسانس صمغ بنه بهعنوان یک ماده ضدمیکروبی طبیعی پتانسیل بالایی برای تولید فیلمهای ضدمیکروبی دارد [50]. بااینحال، مطالعات اندکی درباره خواص ضدباکتریایی و ضدقارچی عصاره بنه بهویژه تأثیر نانوذرات تولیدشده با استفاده از عصاره این گیاه بر باکتری استافیلوکوکوس اورئوس توسط پژوهشگران گزارش شده است. بهدلیل فراوانی استافیلوکوکوس اورئوس در غذا، نقش این میکروارگانیسم را بهعنوان یکی از عوامل مسمومیت نباید نادیده گرفت.
ازآنجاکه انتروتوکسینهای این باکتری در برابر حرارت و پروتئاز مقاوم هستند و در فرایند حرارت و پخت از بین نمیروند، شیوع بالای ژنهای انتروتوکسین در این مطالعه نشاندهنده نقش بالقوه این باکتری در ایجاد مسمومیت غذایی است. افزایش شیوع و مقاومت به سایر آنتیبیوتیکها در سویههای CA.MRSA جداشده از غذا میتواند مشکلی جدی برای سلامت عمومی باشد؛ بنابراین باید برای جلوگیری از آلودگی مواد غذایی و افزایش سطح بهداشت تصمیمات جدی اتخاذ شود [51].
نتایج بررسی حداقل غلظت بازدارندگی و حداقل غلظت باکتریکشی این نوع نانوذره بر روی استافیلوکوکوس اورئوس نشان میدهد این نانوذره اثر بازدارندگی رشد و اثر کشنده بر استافیلوکوکوس اورئوس دارد. با بررسی رشد یا رشد نکردن باکتریها در محیط کشت حاوی نانوذرات، حداقل غلظت بازدارنده تعیین شد. مقایسه اثر ضدباکتریایی نانوذرات بیوسنتزشده با عصاره نشان میدهد اثر ضدباکتریایی نانوذرات بیوسنتزشده با عصاره بنه روی این باکتری بسیار مؤثر است. پیشبینی میشود خواص ضدباکتریایی خوب نانوذرات سنتزشده در این مطالعه بهدلیل وضعیت پایدار نانوذرات تشکیلشده (PDI>0/7>0/1) و توزیع اندازه مناسب نانوذرات بنه باشد [44]. در مطالعه حاضر، در نتایج بهدستآمده از آزمایش قطر متوسط هاله در غلظت 1000 میکروگرم نانوذرات بنه بر روی استافیلوکوک، قطر هاله عدم رشد 12 میلیمتر بود که بیانگر خاصیت ضدمیکروبی عصاره این گیاه است.
املیان و همکاران، سنتز نانوذرات نقره و اثرات آنتیاکسیدانی، سمیت سلولی و ضدباکتریایی آنها در شرایط آزمایشگاهی در عصاره برگ بنه را بررسی کردند و نتایج این مطالعه نشان داد نانوذرات نقره از رشد باکتریها جلوگیری میکند. غلظت 7 میکروگرم بر میلیلیتر و در غلظت 3 تا 15 میکروگرم بر میلیلیتر حذف شد. درنهایت، نانوذرات نقره سنتزشده، غیرسمیت سلولی، فعالیتهای آنتیاکسیدانی و ضدباکتریایی را به روشی وابسته به دُز نشان دادند [2].
صادقی و همکاران، سنتز سبز آسان نانوذرات نقره با استفاده از عصاره آبی گیاه بنه و فعالیت ضدباکتریایی آن را بررسی کردند. نتایج حاکی از آن بود که نانوذرات نقره سنتزشده بهعنوان عامل ضدباکتری مؤثر عمل میکنند. این مطلب که نانوذرات نقره قادر به ارائه اثر ضدباکتریایی بالا هستند و ازاینرو، پتانسیل زیادی در تهیه داروهای استفادهشده در برابر بیماریهای باکتریایی دارند، تأیید شده است.
بهطورکلی باکتریهای گرم مثبت نسبت به باکتریهای گرم منفی به عصارهها و اسانسهای گیاهی حساسیت بیشتری دارند. باتوجهبه اینکه باکتریهای گرم منفی در اطراف دیواره سلولی خود یک لایه بیرونی دارند و بهعنوان مانع عمل کرده و دسترسی ترکیبات آبگریز را محدود میکنند؛ بنابراین از حساسیت کمتری برخوردارند. یافتههای این مطالعه با نتایج سایر پژوهشگران سازگار بود [52].
باتوجهبه در دسترس بودن گیاهان مورد مطالعه در کشور ما و امکان تهیه آن با هزینه کمتر نسبت به سایر داروها و همچنین بهدلیل خواص ضدباکتریایی نانوذرات بیوسنتزشده با عصاره این گیاهان، نتایج چنین تحقیقاتی میتواند مورد توجه پژوهشگران، کارشناسان و تولیدکنندگان دارو بوده و برای مبارزه با عفونتهای ناشی از این باکتریها استفاده شود. در بین روشهای تولید نانوذرات، روش تولید سبز، ارزان، کمخطر و سازگار با محیطزیست است. نانوذرات نقره تولیدشده با این روش بهدلیل استفاده نکردن از مواد شیمیایی خطرناک، قابلیت استفاده در صنایع مرتبط با سلامت انسان را دارند. پس ترکیبی از عوامل ذکرشده باعث شد که نانوذرات نقره بهدستآمده با استفاده از عصاره این گیاه اثرات بازدارندگی خوبی بر استافیلوکوکوس اورئوس داشته باشد.
باتوجهبه مطالعات فوق میتوان نتیجه گرفت که گیاه بنه بهدلیل داشتن خواص غذایی و دارویی بالا میتواند بهعنوان گزینهای مناسب در تولید نانوذرات به روش سبز و کاربرد آن در صنایع مرتبط با سلامت انسان مانند بهداشت و درمان مواد غذایی مورد توجه قرار گیرد. نتایج این تحقیق نشان داد عصاره بنه در زمان کوتاهی قادر به کاهش یونهای نقره بهصورت نانوذرات با توزیع اندازه ذرات مناسب و پایدار است که خاصیت بازدارندگی و کشنده خوبی بر روی استافیلوکوکوس اورئوس دارد؛ بنابراین مطالعه پتانسیل عصاره بنه میتواند راهحلی برای استفاده مؤثر از آن و راهی ارزان و زیستسازگار برای تولید نانوذرات باشد.
باتوجهبه نتایج بهدستآمده در این مطالعه و اثر ضدمیکروبی خوب نانوذرات بنه بر استافیلوکوکوس اورئوس، روشهای کاهش اندازه نانوذرات نقره بنه و ارزیابی آن با سایر روشهای اندازهگیری نانوذرات و اثر ضدمیکروبی آن، توصیه میشود در مورد سایر باکتریهای گرم مثبت تحقیقات بیشتری انجام شود و از این گیاه منحصربهفرد استفاده بهینه شود.
ملاحظات اخلاقی
پیروی از اصول اخلاق پژوهش
این پژوهش، کار تحقیقاتی است که در آن ملاحظات اخلاقی وجود نداشت.
حامی مالی
این پژوهش کار گروهی جناب آقای دکتر جلال مردانه عضو گروه میکروبیولوژی، دانشکده پزشکی، مرکز تحقیقات بیماریهای عفونی، دانشگاه علوم پزشکی گناباد، الهه مرادی، دانشآموخته کارشناسی ارشد علوم و صنایع غذایی و دانشآموزان دبیرستان شاهد ریحانهالنبی شهرستان گناباد است که با حمایت مالی مدیریت محترم دبیرستان شاهد ریحانهالنبی انجام شده است.
مشارکت نویسندگان
مفهومپردازی، تحلیل دادهها و روششناسی: الهه مرادی؛ تحقیق، گردآوری اطلاعات، نگارش پیشنویس و اصلی، منابع مالی و ویرایش منابع: همه نویسندگان.
تعارض منافع
بنابر اظهار نویسندگان، این مقاله تعارض منافع ندارد.
تشکر و قدردانی
نویسندگان از مدیریت دبیرستان دخترانه ریحانهالنبی شهرستان گناباد، خانم مرادی تقدیر و تشکر میکنند. همچنین از همکاری ریاست محترم آزمایشگاه مرکزی پژوهشکده علوم و صنایع غذایی خراسان رضوی، فیضی و همکاران آنها قدردانی میشود.
References
1.Ponce Del Castillo. The European and member states’ approaches to regulating nanomaterials: Two levels of governance. Nanoethics. 2013; 7:189–99. [DOI:10.1007/s11569-013-0181-7]
2.Dwivedi AD, Gopal K. Biosynthesis of silver and gold nanoparticles using Chenopodium album leaf extract. Colloids and Surfaces A: Physicochemical and Engineering Aspects. 2010; 369(1-3):27-33.[DOI:10.1016/j.colsurfa.2010.07.020]
3.Martin-Sanchez F, Maojo V. Biomedical informatics and the convergence of Nano-Bio-Info-Cogno (NBIC) technologies. Yearb Med Inform. 2009; 134-42. [PMID]
4.Shah M, Fawcett D, Sharma S, Tripathy SK, Poinern GEJ. Green synthesis of metallic nanoparticles via biological entities. Materials. 2015; 8(11):7278-308. [DOI:10.3390/ma8115377] [PMID] [PMCID]
5.Makarov VV, Love AJ, Sinitsyna OV, Makarova SS, Yaminsky IV, Taliansky ME, et al. Green nanotechnologies: Synthesis of metal nanoparticlesusing plants. Acta Naturae. 2014; 6(1):35-44. [DOI:10.32607/20758251-2014-6-1-35-44] [PMID] [PMCID]
6.Shankar SS, Rai A, Ahmad A, Sastry M. Rapid synthesis of Au, Ag, and bimetallic Au core-Ag shell nanoparticles using Neem (Azadirachta indica) leaf broth. Journal of Colloid and Interface Science. 2004; 275(2):496-502. [DOI:10.1016/j.jcis.2004.03.003] [PMID]
7.Singh M, Kumar M, Kalaivani R, Manikandan S, Kumaraguru AK. Metallic silver nanoparticle: A therapeutic agent in combination with antifungal drug against human fungal pathogen. Bioprocess and Biosystems Engineering. 2013; 36(4):407-15. [DOI:10.1007/s00449-012-0797-y] [PMID]
8.Protima R, Rauwel E. Emerging trends in nanoparticle synthesis using plant extracts for biomedical applications. Globalal Journal of Nanomedicine. 2017; 1(3):555562. [DOI:10.19080/GJN.2017.01.555562]
9.Li X, Xu H, Chen ZS, Chen G. Biosynthesis of nanoparticles by microorganisms and their applications. Journal of Nanomaterials. 2011; 2011:1-16. [DOI:10.1155/2011/270974]
10.Roy N, Barik A. Green synthesis of silver nanoparticles from the unexploited weed resources. International Journal of Nanotechnology and Applications. 2010; 4(2):95-101. [Link]
11.Percival SL, Bowler PG, Dolman J. Antimicrobial activity of silver-containing dressings on wound microorganisms using an in vitro biofilm model. International Wound Journal. 2007; 4(2):186-91. [DOI:10.1111/j.1742-481X.2007.00296.x] [PMID] [PMCID]
12.Guzman M, Dille J, Godet S. Synthesis and antibacterial activity of silver nanoparticles against gram-positive and gram-negative bacteria. Nanomedicine: Nanotechnology, Biology and Medicine. 2012; 8(1):37-45. [PMID]
13.Pal S, Tak YK, Song JM. Does the antibacterial activity of silver nanoparticles depend on the shape of the nanoparticle? A study of the gram-negative bacterium Escherichia coli. Applied and Environmental Microbiology. 2007; 73(6):1712-20. [PMID] [PMCID]
14.Espinosa-Cristóbal LF, Martínez-Castañón GA, Martínez-Martínez RE, Loyola-Rodriguez JP, Patino-Marin N, Reyes-Macías JF, et al. Antibacterial effect of silver nanoparticles against Streptococcus mutans. Materials Letters. 2009; 63(29):2603-6. [DOI:10.1016/j.matlet.2009.09.018]
15.Gnanadesigan M, Anand M, Ravikumar S, Maruthupandy M, Ali SM, Vijayakumar V, et al. Antibacterial potential of biosynthesised silver nanoparticles using Avicennia marina mangrove plant. Applied Nanoscience. 2012; 2:143–7. [DOI:10.1007/s13204-011-0048-6]
16.Jafari Kokhdan A, Zarifian A. [Floristic study of saverz mountain in kohgiloyeh and boyerahmad province (Persian)]. Journal of Plant Research (Iranian Journal of Biology). 2016; 28(5):929-51. [Link]
17.Doosti B. [The comparison of antibacterial and antifungal effects of Pistacia atlantica gum with some inuse antibiotics (Persian)]. Journal of Cellular and Molecular Research (Iranian Journal of Biology). 2019; 32(1):115-24. [Link]
18.Kiaei E, Mazandarani MA, Ghaemi E. Antibacterial activity of 7 species of medicinal plants on bacteria isolated from UTI patients in Golestan province. Journal of Medicinal plants. 2010; 9(34). [Link]
19.Nejati V, Khaneshi F. [Effect of hydro-alcoholic extract of plantago major leaf on serum level of insulin, glucose, and histology of pancreas and kidney in streptozotocin-induced diabetic rats (Persian)]. Qom University of Medical Sciences Journal. 2013; 7(5):14-20. [Link]
20.Hennekinne JA, De Buyser ML, Dragacci S. Staphylococcus aureus and its food poisoning toxins: Characterization and outbreak investigation. FEMS Microbiology Reviews. 2012; 36(4):815-36. [DOI:10.1111/j.1574-6976.2011.00311.x] [PMID]
21.Roesch M, Perreten V, Doherr MG, Schaeren W, Schällibaum M, Blum JW. Comparison of antibiotic resistance of udder pathogens in dairy cows kept on organic and on conventional farms. Journal of Dairy Science. 2006; 89(3):989-97. [DOI:10.3168/jds.S0022-0302(06)72164-6]
22.Bennett RW, Yeterian M, Smith W, Coles CM, Sassaman M, McClure FD. Staphylococcus aureus identification characteristics and enterotoxigenicity. Journal of Food Science. 1986; 51(5):1337-39. [DOI:10.1111/j.1365-2621.1986.tb13117.x]
23.Imani Fouladi AA, Choupani A, Fallah Mehrabadi J. [Study of prevalence of Enterotoxin type B gene in Meticillin Resistant Staphylococcus aureus (MRSA) isolated from wound (Persian)]. Kowsar Medical Journal. 2011; 16(1):21-5. [Link]
24.Charlebois ED, Perdreau-Remington F, Kreiswirth B, Bangsberg DR, Ciccarone D, Diep BA, et al. Erratum: Origins of community strains of methicillin-resistant Staphylococcus aureus. Clinical Infectious Disease. 2004; 39(1):47-54. [PMID]
25.Kannan RRR, Arumugam R, Ramya D, Manivannan, Anantharaman P. Green synthesis of silver nanoparticles using marine macroalga Chaetomorpha linum. Applied Nanoscience. 2013; 3:229-33. [DOI:10.1007/s13204-012-0125-5]
26.Houshmand B, Mortazavi H, Alikhani Y, Abdolsamadi H, AhmadiMotemayel F, ZareMahmoudabadi R. [In vitro evaluation of antibacterial effect of myrtus extract with different concentrations on some oral bacteria (Persian)]. Journal of Mashhad Dental School. 2011; 35(2):123-30. [DOI:10.22038/JMDS.2011.970]
27.Kermanshah H, Hashemi Kamangar S, Arami S, Mirsalehian A, Kamalinegad M, Karimi M et al. [Comparison of antibacterial effect of hydroalcoholic extract of four plants against cariogenic microorganisms by two in vitro Methods (Persian)]. Journal of Babol University of Medical Sciences. 2011; 13(6):21-9. [Link]
28.Shahverdi AR, Minaeian S, Shahverdi HR, Jamalifar H, Nohi AA. Rapid synthesis of silver nanoparticles using culture supernatants of Enterobacteria: A novel biological approach. Process Biochemistry. 2007; 42(5):919-23. [DOI:10.1016/j.procbio.2007.02.005]
29.Mahmoudi R, Ehsani PA, Tajik H, Akhoundzadeh BA, Khosroshahi A. [Antimicrobial effects of Mentha longifolia L. essential oil and Lactobacillus casei against Staphylococcus aureus in Iranian white cheese (Persian)]. Journal of Food Research. 2010; 3(1):147-61.[Link]
30.Ghodrat IZ, Divsalar A, Ayrian S, Saeidifar M. [Evaluation of the anticancer effects of Samarium nanoparticles synthesized by extract of ginger on HCT116 colorectal cancer cells (Persian)]. Journal of Cell & Tissue. 2020; 10(4):202-13. [Link]
31.Stetefeld J, McKenna SA, Patel TR. Dynamic light scattering: A practical guide and applications in biomedical sciences. Biophysical Reviews. 2016; 8(4):409-27. [PMID] [PMCID]
32.Singh LP, Bhattacharyya SK, Kumar R, Mishra G, Sharma U, Singh G, et al. Sol-Gel processing of silica nanoparticles and their applications.Advances in Colloid and interface Science. 2014; 214:17-37. [PMID]
33.Esmaile F, Koohestani H, Abdollah-Pour H. Characterization and antibacterial activity of silver nanoparticles green synthesized using Ziziphora clinopodioides extract. Environmental Nanotechnology, Monitoring & Management. 2020; 14:100303. [DOI:10.1016/j.enmm.2020.100303]
34.Kavoosi S, Yaghoubi H. [Synthesis of silver nanoparticles using green method of plant extract european marjoram (origanum majorana) and their antibacterial effects (Persian)]. Journal of Cellular and Molecular Research (Iranian Journal of Biology). 2017; 30(2):161-73. [Link]
35.Mittal AK, Chisti Y, Banerjee UC. Synthesis of metallic nanoparticles using plant extracts. Biotechnology Advances. 2013; 31(2):346-56. [PMID]
36.Sivaraman SK, Elango I, Kumar S, Santhanam V. A green protocol for room temperature synthesis of silver nanoparticles in seconds.Current Science (00113891). 2009; 97(7):1055-9. [Link]
37.Sathyavathi R, Krishna MB, Rao SV, Saritha R, Rao DN. Biosynthesis of silver nanoparticlesusing Coriandrum sativum leaf extract and their application in nonlinear optic. Advanced science letters. 2010; 3(2):138-43. [DOI:10.1166/asl.2010.1099]
38.Nikbakht MR, Soleimani Z, Moravveji SA, Esalatmanesh K. [Evaluating the effectiveness of Pistacia atlantica in the improvement of diabetic foot (Persian)]. Feyz. 2016; 20(4):347-51. [Link]
39.Talpur AD. Mentha piperita (Peppermint) as feed additive enhanced growth performance, survival, immune response and disease resistance ofAsian seabass, Lates calcarifer (Bloch) against Vibrio harveyi infection. Aquaculture. 2014; 420-421:71-8. [DOI:10.1016/j.aquaculture.2013.10.039]
40.Douglas JA, Douglas MH, Lauren DR, Martin RJ, Deo B, Follett JM, et al. Effect of plant density and depth of harvest on the production and quality of licorice (Glycyrrhiza glabra) root harvested over 3 years. New Zealand Journal of Crop and Horticultural Science. 2004; 32(4):363-73. [DOI:10.1080/01140671.2004.9514317]
41.Jegadeeswaran P, Shivaraj R, Venckatesh R. Green synthesis of silver nanoparticles from extract of Padina tetrastromatica leaf. Digest Journal of Nanomaterials and Biostructures. 2012; 7(3):991-8. [Link]
42.Reddy GR, Gandhi NN. Environmental friendly biosynthesis, characterization and antibacterial activity of silver nanoparticles by using Senna Saimea plant leaf aqueous extract. Int J Iins Pharm Life Sci. 2012; 2(1):186-93. [Link]
43.Zeng Q, Jiang X, Yu A, Lu GM. Growth mechanisms of silver nanoparticles: A molecular dynamics study. Nanotechnology. 2007; 18(3):035708. [PMID]
44.Ragheb G, Najmoddin N, Aleemardani M. [The effect of synthesis parameters on the particle size, particle size distribution and hydrodynamic diameter of silica nanoparticles via modified StÖber method (Persian)]. Nanomaterials. 2018; 10(34):117-28. [Link]
45.Razmi A, Nikkhah M, Bagheri A, Malekzadeh Shafaroudi S, Shams bakhsh M. [Green syntesis of spherical gold nano particle by Water cress (Persian)]. Modares Journal of Biotechnology. 2017; 8(1):60-70. [Link]
46.Moadi T, Ghahremanzadeh R, Yosefi M, Mohammadi F. [Synthesis of silver nanoparticles (Ag NPs) via four kinds of plants extract and investigation of antimicrobial activity of these nanoparticles (Persian)]. Nashrieh Shimi va Mohandesi Shimi Iran. 2014; 33(4):1-9. [Link]
47.Jansen WT, van der Bruggen JT, Verhoef J, Fluit AC. Bacterial resistance: A sensitive issue complexity of the challenge and containment strategy in Europe. Drug Resistance Updates. 2006; 9(3):123-33. [PMID]
48.Moghtader M, Salari H, Mozafari H, Farahmand A. [Evaluation the qualitative and quantitative essential oil of Calendula officinalis and its antibacterial effects (Persian)]. Journal of Molecular and Cellular Research. 2016; 29(3):331-9. [Link]
49.Panahi M, Barzegar H, Hojjati M. [Effect of pistacia atlantica gum oil on antimicrobial and antioxidant properties of edible starch film (Persian)]. Innovative Food Technologies. 2017; 5(1):77-89. [DOI:10.22104/jift.2017.462]
50.Alizadeh V, , Barzegar H, Nasehi B, Samavati V. [Characterization of physical and antimicrobial properties of chitosan edible films containing pistacia atlantica gum essence (Persian)]. Iranian Food Science and Technology Research. 2017; 13(4):584 -93. [Link]
51.Hoseiyni SM, Arabestani MR, Mahmoodi H, Farhangara E. [Prevalence of G, H, I, J Enterotoxin Genes and Antibacterial Susceptibility Pattern in Staphylococcus aureus strains Isolated from Different Foods (Persian)]. Journal of Mazandaran University of Medical Sciences. 2015; 25(123):1-10. [Link]
2.Dwivedi AD, Gopal K. Biosynthesis of silver and gold nanoparticles using Chenopodium album leaf extract. Colloids and Surfaces A: Physicochemical and Engineering Aspects. 2010; 369(1-3):27-33.[DOI:10.1016/j.colsurfa.2010.07.020]
3.Martin-Sanchez F, Maojo V. Biomedical informatics and the convergence of Nano-Bio-Info-Cogno (NBIC) technologies. Yearb Med Inform. 2009; 134-42. [PMID]
4.Shah M, Fawcett D, Sharma S, Tripathy SK, Poinern GEJ. Green synthesis of metallic nanoparticles via biological entities. Materials. 2015; 8(11):7278-308. [DOI:10.3390/ma8115377] [PMID] [PMCID]
5.Makarov VV, Love AJ, Sinitsyna OV, Makarova SS, Yaminsky IV, Taliansky ME, et al. Green nanotechnologies: Synthesis of metal nanoparticlesusing plants. Acta Naturae. 2014; 6(1):35-44. [DOI:10.32607/20758251-2014-6-1-35-44] [PMID] [PMCID]
6.Shankar SS, Rai A, Ahmad A, Sastry M. Rapid synthesis of Au, Ag, and bimetallic Au core-Ag shell nanoparticles using Neem (Azadirachta indica) leaf broth. Journal of Colloid and Interface Science. 2004; 275(2):496-502. [DOI:10.1016/j.jcis.2004.03.003] [PMID]
7.Singh M, Kumar M, Kalaivani R, Manikandan S, Kumaraguru AK. Metallic silver nanoparticle: A therapeutic agent in combination with antifungal drug against human fungal pathogen. Bioprocess and Biosystems Engineering. 2013; 36(4):407-15. [DOI:10.1007/s00449-012-0797-y] [PMID]
8.Protima R, Rauwel E. Emerging trends in nanoparticle synthesis using plant extracts for biomedical applications. Globalal Journal of Nanomedicine. 2017; 1(3):555562. [DOI:10.19080/GJN.2017.01.555562]
9.Li X, Xu H, Chen ZS, Chen G. Biosynthesis of nanoparticles by microorganisms and their applications. Journal of Nanomaterials. 2011; 2011:1-16. [DOI:10.1155/2011/270974]
10.Roy N, Barik A. Green synthesis of silver nanoparticles from the unexploited weed resources. International Journal of Nanotechnology and Applications. 2010; 4(2):95-101. [Link]
11.Percival SL, Bowler PG, Dolman J. Antimicrobial activity of silver-containing dressings on wound microorganisms using an in vitro biofilm model. International Wound Journal. 2007; 4(2):186-91. [DOI:10.1111/j.1742-481X.2007.00296.x] [PMID] [PMCID]
12.Guzman M, Dille J, Godet S. Synthesis and antibacterial activity of silver nanoparticles against gram-positive and gram-negative bacteria. Nanomedicine: Nanotechnology, Biology and Medicine. 2012; 8(1):37-45. [PMID]
13.Pal S, Tak YK, Song JM. Does the antibacterial activity of silver nanoparticles depend on the shape of the nanoparticle? A study of the gram-negative bacterium Escherichia coli. Applied and Environmental Microbiology. 2007; 73(6):1712-20. [PMID] [PMCID]
14.Espinosa-Cristóbal LF, Martínez-Castañón GA, Martínez-Martínez RE, Loyola-Rodriguez JP, Patino-Marin N, Reyes-Macías JF, et al. Antibacterial effect of silver nanoparticles against Streptococcus mutans. Materials Letters. 2009; 63(29):2603-6. [DOI:10.1016/j.matlet.2009.09.018]
15.Gnanadesigan M, Anand M, Ravikumar S, Maruthupandy M, Ali SM, Vijayakumar V, et al. Antibacterial potential of biosynthesised silver nanoparticles using Avicennia marina mangrove plant. Applied Nanoscience. 2012; 2:143–7. [DOI:10.1007/s13204-011-0048-6]
16.Jafari Kokhdan A, Zarifian A. [Floristic study of saverz mountain in kohgiloyeh and boyerahmad province (Persian)]. Journal of Plant Research (Iranian Journal of Biology). 2016; 28(5):929-51. [Link]
17.Doosti B. [The comparison of antibacterial and antifungal effects of Pistacia atlantica gum with some inuse antibiotics (Persian)]. Journal of Cellular and Molecular Research (Iranian Journal of Biology). 2019; 32(1):115-24. [Link]
18.Kiaei E, Mazandarani MA, Ghaemi E. Antibacterial activity of 7 species of medicinal plants on bacteria isolated from UTI patients in Golestan province. Journal of Medicinal plants. 2010; 9(34). [Link]
19.Nejati V, Khaneshi F. [Effect of hydro-alcoholic extract of plantago major leaf on serum level of insulin, glucose, and histology of pancreas and kidney in streptozotocin-induced diabetic rats (Persian)]. Qom University of Medical Sciences Journal. 2013; 7(5):14-20. [Link]
20.Hennekinne JA, De Buyser ML, Dragacci S. Staphylococcus aureus and its food poisoning toxins: Characterization and outbreak investigation. FEMS Microbiology Reviews. 2012; 36(4):815-36. [DOI:10.1111/j.1574-6976.2011.00311.x] [PMID]
21.Roesch M, Perreten V, Doherr MG, Schaeren W, Schällibaum M, Blum JW. Comparison of antibiotic resistance of udder pathogens in dairy cows kept on organic and on conventional farms. Journal of Dairy Science. 2006; 89(3):989-97. [DOI:10.3168/jds.S0022-0302(06)72164-6]
22.Bennett RW, Yeterian M, Smith W, Coles CM, Sassaman M, McClure FD. Staphylococcus aureus identification characteristics and enterotoxigenicity. Journal of Food Science. 1986; 51(5):1337-39. [DOI:10.1111/j.1365-2621.1986.tb13117.x]
23.Imani Fouladi AA, Choupani A, Fallah Mehrabadi J. [Study of prevalence of Enterotoxin type B gene in Meticillin Resistant Staphylococcus aureus (MRSA) isolated from wound (Persian)]. Kowsar Medical Journal. 2011; 16(1):21-5. [Link]
24.Charlebois ED, Perdreau-Remington F, Kreiswirth B, Bangsberg DR, Ciccarone D, Diep BA, et al. Erratum: Origins of community strains of methicillin-resistant Staphylococcus aureus. Clinical Infectious Disease. 2004; 39(1):47-54. [PMID]
25.Kannan RRR, Arumugam R, Ramya D, Manivannan, Anantharaman P. Green synthesis of silver nanoparticles using marine macroalga Chaetomorpha linum. Applied Nanoscience. 2013; 3:229-33. [DOI:10.1007/s13204-012-0125-5]
26.Houshmand B, Mortazavi H, Alikhani Y, Abdolsamadi H, AhmadiMotemayel F, ZareMahmoudabadi R. [In vitro evaluation of antibacterial effect of myrtus extract with different concentrations on some oral bacteria (Persian)]. Journal of Mashhad Dental School. 2011; 35(2):123-30. [DOI:10.22038/JMDS.2011.970]
27.Kermanshah H, Hashemi Kamangar S, Arami S, Mirsalehian A, Kamalinegad M, Karimi M et al. [Comparison of antibacterial effect of hydroalcoholic extract of four plants against cariogenic microorganisms by two in vitro Methods (Persian)]. Journal of Babol University of Medical Sciences. 2011; 13(6):21-9. [Link]
28.Shahverdi AR, Minaeian S, Shahverdi HR, Jamalifar H, Nohi AA. Rapid synthesis of silver nanoparticles using culture supernatants of Enterobacteria: A novel biological approach. Process Biochemistry. 2007; 42(5):919-23. [DOI:10.1016/j.procbio.2007.02.005]
29.Mahmoudi R, Ehsani PA, Tajik H, Akhoundzadeh BA, Khosroshahi A. [Antimicrobial effects of Mentha longifolia L. essential oil and Lactobacillus casei against Staphylococcus aureus in Iranian white cheese (Persian)]. Journal of Food Research. 2010; 3(1):147-61.[Link]
30.Ghodrat IZ, Divsalar A, Ayrian S, Saeidifar M. [Evaluation of the anticancer effects of Samarium nanoparticles synthesized by extract of ginger on HCT116 colorectal cancer cells (Persian)]. Journal of Cell & Tissue. 2020; 10(4):202-13. [Link]
31.Stetefeld J, McKenna SA, Patel TR. Dynamic light scattering: A practical guide and applications in biomedical sciences. Biophysical Reviews. 2016; 8(4):409-27. [PMID] [PMCID]
32.Singh LP, Bhattacharyya SK, Kumar R, Mishra G, Sharma U, Singh G, et al. Sol-Gel processing of silica nanoparticles and their applications.Advances in Colloid and interface Science. 2014; 214:17-37. [PMID]
33.Esmaile F, Koohestani H, Abdollah-Pour H. Characterization and antibacterial activity of silver nanoparticles green synthesized using Ziziphora clinopodioides extract. Environmental Nanotechnology, Monitoring & Management. 2020; 14:100303. [DOI:10.1016/j.enmm.2020.100303]
34.Kavoosi S, Yaghoubi H. [Synthesis of silver nanoparticles using green method of plant extract european marjoram (origanum majorana) and their antibacterial effects (Persian)]. Journal of Cellular and Molecular Research (Iranian Journal of Biology). 2017; 30(2):161-73. [Link]
35.Mittal AK, Chisti Y, Banerjee UC. Synthesis of metallic nanoparticles using plant extracts. Biotechnology Advances. 2013; 31(2):346-56. [PMID]
36.Sivaraman SK, Elango I, Kumar S, Santhanam V. A green protocol for room temperature synthesis of silver nanoparticles in seconds.Current Science (00113891). 2009; 97(7):1055-9. [Link]
37.Sathyavathi R, Krishna MB, Rao SV, Saritha R, Rao DN. Biosynthesis of silver nanoparticlesusing Coriandrum sativum leaf extract and their application in nonlinear optic. Advanced science letters. 2010; 3(2):138-43. [DOI:10.1166/asl.2010.1099]
38.Nikbakht MR, Soleimani Z, Moravveji SA, Esalatmanesh K. [Evaluating the effectiveness of Pistacia atlantica in the improvement of diabetic foot (Persian)]. Feyz. 2016; 20(4):347-51. [Link]
39.Talpur AD. Mentha piperita (Peppermint) as feed additive enhanced growth performance, survival, immune response and disease resistance ofAsian seabass, Lates calcarifer (Bloch) against Vibrio harveyi infection. Aquaculture. 2014; 420-421:71-8. [DOI:10.1016/j.aquaculture.2013.10.039]
40.Douglas JA, Douglas MH, Lauren DR, Martin RJ, Deo B, Follett JM, et al. Effect of plant density and depth of harvest on the production and quality of licorice (Glycyrrhiza glabra) root harvested over 3 years. New Zealand Journal of Crop and Horticultural Science. 2004; 32(4):363-73. [DOI:10.1080/01140671.2004.9514317]
41.Jegadeeswaran P, Shivaraj R, Venckatesh R. Green synthesis of silver nanoparticles from extract of Padina tetrastromatica leaf. Digest Journal of Nanomaterials and Biostructures. 2012; 7(3):991-8. [Link]
42.Reddy GR, Gandhi NN. Environmental friendly biosynthesis, characterization and antibacterial activity of silver nanoparticles by using Senna Saimea plant leaf aqueous extract. Int J Iins Pharm Life Sci. 2012; 2(1):186-93. [Link]
43.Zeng Q, Jiang X, Yu A, Lu GM. Growth mechanisms of silver nanoparticles: A molecular dynamics study. Nanotechnology. 2007; 18(3):035708. [PMID]
44.Ragheb G, Najmoddin N, Aleemardani M. [The effect of synthesis parameters on the particle size, particle size distribution and hydrodynamic diameter of silica nanoparticles via modified StÖber method (Persian)]. Nanomaterials. 2018; 10(34):117-28. [Link]
45.Razmi A, Nikkhah M, Bagheri A, Malekzadeh Shafaroudi S, Shams bakhsh M. [Green syntesis of spherical gold nano particle by Water cress (Persian)]. Modares Journal of Biotechnology. 2017; 8(1):60-70. [Link]
46.Moadi T, Ghahremanzadeh R, Yosefi M, Mohammadi F. [Synthesis of silver nanoparticles (Ag NPs) via four kinds of plants extract and investigation of antimicrobial activity of these nanoparticles (Persian)]. Nashrieh Shimi va Mohandesi Shimi Iran. 2014; 33(4):1-9. [Link]
47.Jansen WT, van der Bruggen JT, Verhoef J, Fluit AC. Bacterial resistance: A sensitive issue complexity of the challenge and containment strategy in Europe. Drug Resistance Updates. 2006; 9(3):123-33. [PMID]
48.Moghtader M, Salari H, Mozafari H, Farahmand A. [Evaluation the qualitative and quantitative essential oil of Calendula officinalis and its antibacterial effects (Persian)]. Journal of Molecular and Cellular Research. 2016; 29(3):331-9. [Link]
49.Panahi M, Barzegar H, Hojjati M. [Effect of pistacia atlantica gum oil on antimicrobial and antioxidant properties of edible starch film (Persian)]. Innovative Food Technologies. 2017; 5(1):77-89. [DOI:10.22104/jift.2017.462]
50.Alizadeh V, , Barzegar H, Nasehi B, Samavati V. [Characterization of physical and antimicrobial properties of chitosan edible films containing pistacia atlantica gum essence (Persian)]. Iranian Food Science and Technology Research. 2017; 13(4):584 -93. [Link]
51.Hoseiyni SM, Arabestani MR, Mahmoodi H, Farhangara E. [Prevalence of G, H, I, J Enterotoxin Genes and Antibacterial Susceptibility Pattern in Staphylococcus aureus strains Isolated from Different Foods (Persian)]. Journal of Mazandaran University of Medical Sciences. 2015; 25(123):1-10. [Link]
52.Alizadeh Behbahani B, Shahidi F, Tabatabaei Yazdi F, Mortazavi SA, Mohebbi M. [The antimicrobial effect and interaction of aqueous and ethanolic extracts of Plantago major on Staphylococcus aureus, Listeria inocua, Escherichia coli and Pseudomonas aeruginosa in vitro (Persian)]. Iranian Journal of Infectious Diseases and Tropical Medicine. 2017; 21(75):1-8. [Link] .
نوع مطالعه: پژوهشی |
موضوع مقاله:
پزشكي آزمايشگاهی
دریافت: 1400/3/3 | پذیرش: 1400/6/27 | انتشار: 1400/12/10
دریافت: 1400/3/3 | پذیرش: 1400/6/27 | انتشار: 1400/12/10
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |