دوره 26، شماره 2 - ( بهار 1399 )
جلد 26 شماره 2 صفحات 155-142 |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Aboeepoor S, Dehghani Ashkezari M, Aboee-Mehrizi F, Haghiralsadat B F, Nikoonahad Lotfabadi N. Designing and Characterizing Nano-carriers Containing Nepeta Persica Extract and Their Effect on Bone Cancer. Intern Med Today 2020; 26 (2) :142-155
URL: http://imtj.gmu.ac.ir/article-1-3312-fa.html
URL: http://imtj.gmu.ac.ir/article-1-3312-fa.html
ابوئیپور سمانه، دهقانی اشکذری محمود، ابویی مهریزی فاطمه، حقیرالسادات بی بی فاطمه، نیکونهاد لطف آبادی نرگس. طراحی و مشخصهیابی حامل نانویی حاوی عصاره Nepeta persica و تأثیر آن بر سرطان استخوان (رده سلولی MG-63). طب داخلی روز. 1399; 26 (2) :142-155
سمانه ابوئیپور1 

 ، محمود دهقانی اشکذری1
، محمود دهقانی اشکذری1 

 ، فاطمه ابویی مهریزی*2
، فاطمه ابویی مهریزی*2 

 ، بی بی فاطمه حقیرالسادات3
، بی بی فاطمه حقیرالسادات3 

 ، نرگس نیکونهاد لطف آبادی4
، نرگس نیکونهاد لطف آبادی4 




 ، محمود دهقانی اشکذری1
، محمود دهقانی اشکذری1 

 ، فاطمه ابویی مهریزی*2
، فاطمه ابویی مهریزی*2 

 ، بی بی فاطمه حقیرالسادات3
، بی بی فاطمه حقیرالسادات3 

 ، نرگس نیکونهاد لطف آبادی4
، نرگس نیکونهاد لطف آبادی4 


1- مرکز تحقیقات زیستفناوری پزشکی، دانشگاه آزاد اسلامی، واحد اشکذر، یزد، ایران.
2- دانشکده پزشکی، دانشگاه آزاد اسلامی واحد یزد، یزد، ایران. ،aboeef@yahoo.com
3- مرکز نانوتکنولوژی و مهندسی بافت، پژوهشکده علوم تولید مثل یزد، دانشگاه علومپزشکی شهید صدوقی یزد. یزد، ایران.
4- گروه زیستشناسی، دانشکده علوم پایه، دانشگاه علم و هنر، یزد، ایران.
2- دانشکده پزشکی، دانشگاه آزاد اسلامی واحد یزد، یزد، ایران. ،
3- مرکز نانوتکنولوژی و مهندسی بافت، پژوهشکده علوم تولید مثل یزد، دانشگاه علومپزشکی شهید صدوقی یزد. یزد، ایران.
4- گروه زیستشناسی، دانشکده علوم پایه، دانشگاه علم و هنر، یزد، ایران.
متن کامل [PDF 6187 kb]
(3035 دریافت)
| چکیده (HTML) (3781 مشاهده)

References
Hart BL. The evolution of herbal medicine: Behavioural perspectives. Animal Behaviour. 2005; 70(5):975-89. [DOI:10.1016/j.anbehav.2005.03.005]
Geller DS, Gorlick R. Osteosarcoma: A review of diagnosis, management, and treatment strategies. Clinical Advances in Hematology & Oncology. 2010; 8(10):705-18. [PMID]
Moghassemi S, Hadjizadeh A. Nano-niosomes as nanoscale drug delivery systems: An illustrated review. Journal of Controlled Release. 2014; 185:22-36. [DOI:10.1016/j.jconrel.2014.04.015] [PMID]
Yang XB, Wu WY, Long SQ, Deng H, Pan ZQ. Effect of gefitinib plus Chinese Herbal Medicine (CHM) in patients with advanced non-small-cell lung cancer: A retrospective case-control study. Complementary Therapies in Medicine. 2014; 22(6):1010-8. [DOI:10.1016/j.ctim.2014.10.001] [PMID]
Cragg GM, Newman DJ. Plants as a source of anti-cancer agents. Journal of Ethnopharmacology. 2005; 100(1-2):72-9. [DOI:10.1016/j.jep.2005.05.011] [PMID]
Nobili S, Lippi D, Witort E, Donnini M, Bausi L, Mini E, et al. Natural compounds for cancer treatment and prevention. Pharmacological Research. 2009; 59(6):365-78. [DOI:10.1016/j.phrs.2009.01.017] [PMID]
Evans WC, Evans D, Trease GE. Trease and Evans pharmacognosy. Philadelphia: Saunders/Elsevier; 2009. https://books.google.com/books?id=ujetPwAACAAJ&dq
Baser KHC, Oözek T, Yildiz B, Bahçecioglu Z, Tuümen G. Composition of the essential oil of Nepeta fissa C.A.Meyer. Journal of Essential Oil Research. 2000; 12(1):27-8. [DOI:10.1080/10412905.2000.9712033]
Rapisarda A, Galati EM, Tzakou O, Flores M, Miceli N. Nepeta sibthorpii Bentham (Lamiaceae): Micromorphological analysis of leaves and flowers. Il Farmaco. 2001; 56(5-7):413-5. [DOI:10.1016/S0014-827X(01)01050-3]
Tzakou O, Harvala C, Galati EM, Sanogo R. Essential oil composition of Nepeta argolica Bory et Chaub. subsp. argolica. Flavour and Fragrance Journal. 2000; 15(2):115-8. [DOI:10.1002/(SICI)1099-1026(200003/04)15:2<115::AID-FFJ877>3.0.CO;2-9]
Mozaffarian V. [A dictionary of Iranian plant, names: Latin, English, Persian (Latin-English-Persian)]. 2nd ed. Tehran: Farhang Moaser; 1998. http://opac.nlai.ir/opac-prod/bibliographic/555105
Haghiralsadat F, Amoabediny G, Sheikhha MH, Zandieh-Doulabi B, Naderinezhad S, Helder MN, et al. New liposomal doxorubicin nanoformulation for osteosarcoma: Drug release kinetic study based on thermo and pH sensitivity. Chemical Biology & Drug Design. 2017; 90(3):368-79. [DOI:10.1111/cbdd.12953] [PMID]
Mosmann T. Rapid colorimetric assay for cellular growth and survival: Application to proliferation and cytotoxicity assays. Journal of Immunological Methods. 1983; 65(1-2):55-63. [DOI:10.1016/0022-1759(83)90303-4]
Zarei M, Arjmand M, Mohammadi M, Chiani M, Ebrahimi H, Akbarzadeh Khiavi A. [Preparation of nanoniosomal Paclitaxel formulation and survey of its cytotoxic effect on breast cancer cell line (MCF-7) (Persian)]. New Cellular & Molecular Biotechnology Journal. 2013; 3(12):17-23. http://ncmbjpiau.ir/article-1-438-en.pdf
Khalighi-Sigaroodi F, Ahvazi M, Ebrahimzadeh H, Rahimifard N. [Chemical composition of the essential oil and antioxidant activities, total phenol and flavonoid content of the extract of Nepeta pogonosperma (Persian)]. Journal of Medicinal Plants. 2013; 4(48):185-98. http://jmp.ir/article-1-72-en.html
Shakeri A, Khakdan F, Soheili V, Sahebkar AH, Rassam GA, Asili J. Chemical composition, antibacterial activity, and cytotoxicity of essential oil from Nepeta ucrainica L. spp. kopetdaghensis. Industrial Crops and Products. 2014; 58:315-21. [DOI:10.1016/j.indcrop.2014.04.009]
Moghimipour E, Kouchak M, Bahmandar R. [Nano-liposomes as new drug delivery carriers (Persian)]. Jundishapur Scientific Medical Journal. 2013; 12(5):467-83. http://jsmj.ajums.ac.ir/article_49795_en.html
Tiwari G, Tiwari R, Sriwastawa B, Bhati L, Pandey S, Pandey P, et al. Drug delivery systems: An updated review. International Journal of Pharmaceutical Investigation. 2012; 2(1):2-11. [DOI:10.4103/2230-973X.96920] [PMID] [PMCID]
Fang JY, Hong CT, Chiu WT, Wang YY. Effect of liposomes and niosomes on skin permeation of enoxacin. International Journal of Pharmaceutics. 2001; 219(1-2):61-72. [DOI:10.1016/S0378-5173(01)00627-5]
Mujoriya RZ, Bodla RB. Design and development of niosomal delivery system for ketoprofen. Advances in Life Science and Technology. 2012; 3:1-13. https://www.iiste.org/Journals/index.php/ALST/article/view/963
Srinivas S, Anand Kumar Y, Hemanth A, Anitha M. Preparation and evaluation of niosomes containing aceclofenac. Digest Journal of Nanomaterials and Biostructures. 2010; 5(1):249-54. http://www.chalcogen.ro/249_Srinivas.pdf
Askari M, Nikoonahad Lotfabadi N. [Evaluation of niosomal nano-carriers capabilities on toxicity preservation and delivery of pomegranate peel extract in cell culture conditions (MCF-7 cell line of breast cancer) (Persian)]. Daneshvar Medicine: Basic and Clinical Research Journal. 2018; 26(5):9-20. http://daneshvarmed.shahed.ac.ir/article-1-2015-en.html
Karimi-Moghddam A, Nikoonahad Lotfabadi N, Haghiralsadat BF, Majdizadeh M. [Investigating the effect of lipid nanoparticles containing silibinin anticancer drug on the growth of breast cancer MCF-7 cell line (Persian)]. Journal of Torbat Heydariyeh University of Medical Sciences. 2018; 6(4):1-12. http://jms.thums.ac.ir/article-1-563-en.pdf
Bahrami-Banan F, Sheikhha MH, Ghasemi N, Majdizadeh M, Haghiralsadat BF. [Preparation and study of nano-niosomes containing doxorubicin and evaluation of its toxicity on acute myeloblastic leukemia cell line KG-1 (Persian)]. Journal of Payavard Salamat. 2018; 12(4):309-23. http://payavard.tums.ac.ir/article-1-6592-en.html
Pardakhty A, Shakibaie M, Daneshvar H, Khamesipour A, Mohammadi-Khorsand T, Forootanfar H. Preparation and evaluation of niosomes containing autoclaved Leishmania major : A preliminary study. Journal of Microencapsulation. 2012; 29(3):219-24. [DOI:10.3109/02652048.2011.642016] [PMID]
متن کامل: (4280 مشاهده)
مقدمه
سرطان یکی از مهمترین عوامل مرگومیر در سرتاسر جهان است. هر ساله در دنیا 10 میلیون نفر به سرطان مبتلا میشوند که بیش از نیمی از آنها میمیرند. بر اساس گزارشهای مؤسسه جهانی سرطان، علاوه بر این، نرخ رشد سرطان تا سال 2020 بیش از 50 درصد خواهد بود و به آمار 15 میلیون نفر مبتلا خواهد رسید. با توجه به آمار سالانه مرگومیر سرطان در دنیا از دیرباز دستیابی به روشهای مؤثر و قطعی درمان سرطان یکی از مهمترین دغدغههای محققین بوده است [1]. سرطان استخوان یک تومور مزانشیمی اولیه است که از نظر بافت شناختی با تولید استئوئید توسط سلولهای بدخیم مشخص میشود. این بدخیمی نسبتاً نادر است و تقریباً 900 مورد جدید در سال در ایالات متحده گزارش میشود. علیرغم نادر بودن، استئوسارکوما شایعترین بدخیمی استخوانی است [2].
روشهای درمانی کنونی اغلب با عوارض جانبی شدیدی همراه هستند که گاه از خود بیماری رنجآورتر است. امروزه در داروسازی مدرن تلاشهای زیادی برای بهینه کردن عملکرد فارماکولوژیکی و کاهش اثرات جانبی دارو انجام میشود. متأسفانه به علت جذب پایین دارو در بدن، متابولیسم سریع آن و حذف سریع دارو، غلظت دارو در بدن ثابت نمیماند و علاوه بر آن، بعضی از داروها را، به علت محلولیت پایینشان در آب نمیتوان به صورت تزریق داخل وریدی تجویز کرد. به منظور حل این مشکل از حاملهایی مانند نیوزومها استفاده میشود. ﻧﻴﻮزومها ﺣﺎﻣﻞهای دوﻻﻳﻪای هستند که از هیدراتاسیون کلسترول با سورفکتانتهای غیریونی در محیط آبی تشکیل شده و ﻗﺎدرﻧﺪ ﻣﻮاد را در خود محبوس کنند. از لحاظ حلالیت، نیوزومها طیف وسیعتری از داروها شامل داروهای هیدروفیل و لیپوفیل را به دام میاندازند. نیوزومها به عنوان حاملین دولایه مدلهای ایدهآلی از غشاهای سلولی زیستی هستند که با به حداقل رساندن تاًثیرات مضر بر روی سلامتی سلولها و بافتها عمل میکنند. به دلیل قابلیت زیست سازگاری و زیست تخریبپذیری نانونیوزومها در کنار سایز نانویی، کاربردهای فراوانی در محدوده وسیعی از زمینهها مانند درمان سرطان، در دسترس قرار دادن دارو و ژنها، مواد آرایشی، صنایع غذایی و کشاورزی نشان دادهاند [3].
امروزه گرایش عمومی جامعه به استفاده از داروها و درمانهای گیاهی و به طور کلی فراوردههای طبیعی رو به افزایش بوده به طوری که داروهای گیاهی سهم بزرگی از فراوردههای دارویی تجاری ساختهشده را به خود اختصاص دادهاند [4 ،1]. گیاهان از زمانهای بسیار قدیم برای درمان بیماریهای گوناگون انسان مورد استفاده بودهاند [5]. بررسیهای اخیر نشان میدهد که بیش از 60 درصد درمان سرطانها به وسیله ویتامینها یا گیاهان انجام میشود. این گیاهان علیه انواع مختلفی از تومورها یا سرطانها از قبیل تومور بافت پیوندی، بافت لنفاوی و سرطان خون مورد استفاده هستند [6].
جنس Nepta (از تیره نعناعیان) که در ایران با عنوان پونهسا شناخته میشود، حاوی گونههای مختلف یکساله و چندساله است که در نقاط مختلف آسیا، اروپا و شمال آفریقا یافت میشوند. حدود 250 گونه از این جنس در نقاط مختلف جهان گزارش شدهاند [7]. گونههای مختلف Nepta به طور گستردهای در طب سنتی بسیاری از کشورها به عنوان داروی ضدنفخ، خلطآور، مدر، ضدآسم، ضدعفونیکننده، ضدسرفه، معرق، تقویتکننده قلب و قاعدهآور استفاده میشوند [10-8]. جنس Nepta در ایران دارای 67 گونه است که به صورت وحشی در نقاط مختلف ایران پراکنده بوده و اکثراً بومی هستند [11]. گونه پونهسای ایرانی، از گیاهان بومی ایران است که در مناطق مختلف کشور رشد میکند.
در این تحقیق، خاصیت ضدسرطانی گیاه پونهسای ایرانی در برابر سلولهای سرطانی استخوان مورد مطالعه قرار گرفته است. به منظور بهینهسازی در فرایند دارورسانی به بافت هدف، فرمولاسیونهای مختلفی از نانوحامل نیوزومیحاوی عصاره طراحی شده است و پارامترهای مختلف این سامانهها از قبیل میزان بارگذاری عصاره، میزان و سرعت رهایش عصاره و همچنین میزان سمیت سلولی سامانه در مقابل سلول سرطانی مذکور مورد بررسی قرار گرفته است.
مواد و روشها
منابع گیاهی و عصارهگیری
گیاه پونهسای ایرانی در فصل گلدهی از ایستگاه تحقیقاتی گیاهان دارویی یزد جمعآوری شد و توسط بخش گیاهشناسی مرکز تحقیقات و آموزش کشاورزی و منابع طبیعی دانشگاه یزد مورد شناسایی قرار گرفت. این گونه در هرباریوم مرکز تحقیقات مذکور به شماره هرباریومی 3059 موجود است. گیاه در محیطی سایه و به دور از تابش مستقیم نور خورشید خشک شد. عصارهگیری از گیاه پونهسای ایرانی با استفاده از دستگاه سوکسله انجام پذیرفت. بدین منظور، گیاه خشکشده توسط دستگاه خردکن خانگی آسیاب شد، مقداری از آن جهت عصارهگیری داخل کارتوش بارگذاری شد و در داخل سیستم سوکسله قرار داده شد. از حلال اتانول 70 درصد نیز به عنوان حلال مناسب جهت عصارهگیری استفاده شد. عمل عصارهگیری طی پنج مرحله تکرار شد تا ترکیبات گیاه به طور کامل استخراج شود. بعد از اتمام عصارهگیری، محتویات بالن صاف شد و عصاره حاصل در داخل یک ظرف شیشهای روباز، در مجاورت هوا و به دور از تابش نور خورشید خشک شد. عصاره خشکشده جهت انجام آزمایشات بعدی مورد استفاده قرار گرفت.
تهیه و سنتزنانونیوزوم
از روش آبدهی فیلم نازک که روشی کلاسیک در تهیه وزیکولهاست برای سنتز نانونیوزومها استفاده شد. در این روش، فیلم نازک لیپیدی با تبخیرآمفیفیل درکلروفرم یا اتانول تشکیل میشود. بعد از تماس فیلم نازک با آب، نمونه حل میشود و فاز وزیکولی شکل میگیرد [12].
اختلاط فاز لیپیدی وتشکیل فیلم نازک
فاز لیپیدی شامل کلسترول-Span-60 (سیگما، آمریکا) است. در نمونه اصلی، فاز لیپیدی با چندین نسبت مولی متفاوت به کلروفرم (مرک، آلمان) اضافه و حل شد. اسانس به نسبت یک به 20 به فاز لیپدی اضافه شد. سپس فاز آلی محلول حاصل با استفاده از دستگاه تبخیرکننده دوار (هایدولف، آلمان) در دمای حدود 55 درجه سانتیگراد برای کلروفرم و با دور تقریبی 150 دور در دقیقه، حذف و فیلم نازک لیپیدی تشکیل شد. همچنین جهت اطمینان از حذف کامل حلّال، فیلم نازک لیپیدی چندین دقیقه با گاز نیتروژن هوادهی شد و 24 ساعت در دمای چهار درجه سانتیگراد قرار گرفت.
آبدهی فیلم لیپیدی
در این مرحله آب دیونیزه اضافه شد تا تا فیلم لیپیدی آبدهی شده و به همان غلظت اولیه میلیگرم بر میلیلیتر برسد. برای اختلاط بیشتر بدون روشن کردن خلأ 45 دقیقه تا یک ساعت بالن حاوی محلول فاز آبی به دستگاه تبخیرکننده دوار با دمای 37 درجه سانتیگراد و 150 دور بر دقیقه متصل شد، محلول شیریرنگ حاصل سوسپانسیون نیوزوم، حاوی عصاره است.
کاهش سایز
برای کاهش اندازه نیوزومهای چندلایه بزرگ و تشکیل وزیکولهای کوچک تکلایه از روش سونیکاسیون استفاده شد. پروب دستگاه سونیکاسیون در داخل محلول کلوئیدی نیوزومها قرارداده شد و سپس فرایند سونیکاسیون جهت تولید نیوزومهای تکجداره با توان 40 و 60 درصد (Amplitude) به مدت 10 دقیقه (10 ثانیه روشن و 15 ثانیه خاموش) انجام شد.
علاوه بر کاهش سایز به روش سونیکیت پروبی، میتوان از سونیکیت حمامی (Scientz، چین) نیز استفاده کرد که در این روش محلول کلوئیدی نیوزومها در سونیکیت حمامی قرار داده شده و دستگاه در دمای 37 درجه سانتیگراد نیم ساعت تنظیم میشود.
فرایند فیلتراسیون
قبل از فیلتراسیون، ناخالصی و مواد اضافی نمونهها (همچون تیتانیوم حاصل از سونیکاسیون پروبی) با استفاده از سانتریفیوژ با دور پنج هزار به مدت پنج دقیقه از محلول نیوزومی جداسازی شد. سپس به منظور جداسازی ذرات با اندازه بزرگتر از ذرات کوچکتر و همگن شدن محلول بهدستآمده در مرحله پیشفیلتراسیون از فیلتر 45/0 میکرومتر استفاده شد و در انتها جهت فیلتراسیون استریلکننده، محلول از فیلتر با قطر حفرات 22/0 میکرومتر عبور داده شد.
حذف عصاره آزاد Nepta
پس از بارگذاری عصاره به منظور جدا کردن عصاره بارگذارینشده، نیوزوم داخل کیسه دیالیز سلولزی ریخته شد و در بشر حاوی آب با حجم 150 برابر حجم نیوزوم به مدت دو ساعت در دمای چهار درجه سانتیگراد استیرر شد.
تعیین سایز و محدوده توزیع اندازه نانونیوزومهای حاوی عصاره
محدوده توزیع اندازه ذرات و همچنین پیک اندازه ذرات با استفاده از DLS و دستگاه نانوسایزر Brookhaven Instruments Corp تعیین شد. اندازهگیری نانونیوزومها در یک زاویه 90 درجه و تابش نور لیزر با طول موج 657 نانومتر در دمای 25 درجه سانتیگراد صورت گرفت. همچنین اندازهگیری نمونهها اغلب در پنج مرتبه و هر مرتبه با مدتزمان 30 ثانیه انجام شد. برای تهیه نمونه جهت تعیین اندازه به 600 میکرولیتر محلول با غلظت 5/0 - 1/0 میلیگرم بر میلیلیتر نیاز بود.
تعیین پتانسیل زتا نانونیوزوم
میزان بار سطحی و پتانسیل زتا نانونیوزومهای حامل عصاره با استفاده از دستگاه زتاسایزر شرکت Brookhaven Instruments Corp در دمای 25 درجه سانتیگراد اندازهگیری شد. برای تعیین بار سطحی به 1500 میکرولیتر محلول با غلظت 1/0 میلیگرم بر میلیلیتر نیاز است.
تصویربرداری از نانونیوزوم
از نانو نیوزومها با استفاده از میکروسکوپ الکترونیکی SEM به منظور بررسی شکل ظاهری و ساختار نانونیوزومهای تولیدی حامل عصاره تصویربرداری شد. یک قطره از نمونه با غلظت 1/0 میلیگرم بر میلیلیتر روی لامل ریخته شده شد. روی نمونه پس از خشک شدن، پوشش طلا داده شده و تصویر SEM تهیه شد.
آنالیز نانونیوزوم سنتزشده توسط دستگاه طیفسنجی مادون قرمز
گروههای عاملی سطح نانونیوزوم تولیدشده توسط آنالیز طیفسنجی مادون قرمز (FTIR) بررسی شد. در طیف FTIR عمدتاً دو ناحیه مورد توجه است. ناحیه گروه عاملی از cm-1 1550 تا 4000، ناحیهای است که بیشتر کششهای پیوندی اتفاق میافتد. در این ناحیه معمولاً تعداد نسبتاً کمی پیک وجود دارد. اما بسیاری از پیکهای آن مشخصکننده گروههای عاملی هستند. برای اطمینان از نبود عصاره آزاد و مواد اضافی در نمونه نانونیوزوم، از نمونه دیالیزشده نانونیوزومها، استفاده شد و به منظور کاهش رطوبت، حدود نیمساعت نمونه در آون با دمای تقریبی 60 درجه سانتیگراد قرار داده شد.
بررسی میزان بارگذاری عصاره داخل نیوزوم
به منظور بررسی میزان عصاره بارگذاریشده، نیوزومهای تهیهشده با نسبت یک به 9 با محلول ایزو 2 پروپانول (1 درصد وزنی به حجمی در آب) مخلوط شد و جذب آنها توسط دستگاه اسپکتروفوتومتر اندازه گرفته شد. نهایتاً غلظت عصاره با توجه به معادله نمودار کالیبراسیون و با استفاده از فرمول شماره 1 به دست آمد.
سرطان یکی از مهمترین عوامل مرگومیر در سرتاسر جهان است. هر ساله در دنیا 10 میلیون نفر به سرطان مبتلا میشوند که بیش از نیمی از آنها میمیرند. بر اساس گزارشهای مؤسسه جهانی سرطان، علاوه بر این، نرخ رشد سرطان تا سال 2020 بیش از 50 درصد خواهد بود و به آمار 15 میلیون نفر مبتلا خواهد رسید. با توجه به آمار سالانه مرگومیر سرطان در دنیا از دیرباز دستیابی به روشهای مؤثر و قطعی درمان سرطان یکی از مهمترین دغدغههای محققین بوده است [1]. سرطان استخوان یک تومور مزانشیمی اولیه است که از نظر بافت شناختی با تولید استئوئید توسط سلولهای بدخیم مشخص میشود. این بدخیمی نسبتاً نادر است و تقریباً 900 مورد جدید در سال در ایالات متحده گزارش میشود. علیرغم نادر بودن، استئوسارکوما شایعترین بدخیمی استخوانی است [2].
روشهای درمانی کنونی اغلب با عوارض جانبی شدیدی همراه هستند که گاه از خود بیماری رنجآورتر است. امروزه در داروسازی مدرن تلاشهای زیادی برای بهینه کردن عملکرد فارماکولوژیکی و کاهش اثرات جانبی دارو انجام میشود. متأسفانه به علت جذب پایین دارو در بدن، متابولیسم سریع آن و حذف سریع دارو، غلظت دارو در بدن ثابت نمیماند و علاوه بر آن، بعضی از داروها را، به علت محلولیت پایینشان در آب نمیتوان به صورت تزریق داخل وریدی تجویز کرد. به منظور حل این مشکل از حاملهایی مانند نیوزومها استفاده میشود. ﻧﻴﻮزومها ﺣﺎﻣﻞهای دوﻻﻳﻪای هستند که از هیدراتاسیون کلسترول با سورفکتانتهای غیریونی در محیط آبی تشکیل شده و ﻗﺎدرﻧﺪ ﻣﻮاد را در خود محبوس کنند. از لحاظ حلالیت، نیوزومها طیف وسیعتری از داروها شامل داروهای هیدروفیل و لیپوفیل را به دام میاندازند. نیوزومها به عنوان حاملین دولایه مدلهای ایدهآلی از غشاهای سلولی زیستی هستند که با به حداقل رساندن تاًثیرات مضر بر روی سلامتی سلولها و بافتها عمل میکنند. به دلیل قابلیت زیست سازگاری و زیست تخریبپذیری نانونیوزومها در کنار سایز نانویی، کاربردهای فراوانی در محدوده وسیعی از زمینهها مانند درمان سرطان، در دسترس قرار دادن دارو و ژنها، مواد آرایشی، صنایع غذایی و کشاورزی نشان دادهاند [3].
امروزه گرایش عمومی جامعه به استفاده از داروها و درمانهای گیاهی و به طور کلی فراوردههای طبیعی رو به افزایش بوده به طوری که داروهای گیاهی سهم بزرگی از فراوردههای دارویی تجاری ساختهشده را به خود اختصاص دادهاند [4 ،1]. گیاهان از زمانهای بسیار قدیم برای درمان بیماریهای گوناگون انسان مورد استفاده بودهاند [5]. بررسیهای اخیر نشان میدهد که بیش از 60 درصد درمان سرطانها به وسیله ویتامینها یا گیاهان انجام میشود. این گیاهان علیه انواع مختلفی از تومورها یا سرطانها از قبیل تومور بافت پیوندی، بافت لنفاوی و سرطان خون مورد استفاده هستند [6].
جنس Nepta (از تیره نعناعیان) که در ایران با عنوان پونهسا شناخته میشود، حاوی گونههای مختلف یکساله و چندساله است که در نقاط مختلف آسیا، اروپا و شمال آفریقا یافت میشوند. حدود 250 گونه از این جنس در نقاط مختلف جهان گزارش شدهاند [7]. گونههای مختلف Nepta به طور گستردهای در طب سنتی بسیاری از کشورها به عنوان داروی ضدنفخ، خلطآور، مدر، ضدآسم، ضدعفونیکننده، ضدسرفه، معرق، تقویتکننده قلب و قاعدهآور استفاده میشوند [10-8]. جنس Nepta در ایران دارای 67 گونه است که به صورت وحشی در نقاط مختلف ایران پراکنده بوده و اکثراً بومی هستند [11]. گونه پونهسای ایرانی، از گیاهان بومی ایران است که در مناطق مختلف کشور رشد میکند.
در این تحقیق، خاصیت ضدسرطانی گیاه پونهسای ایرانی در برابر سلولهای سرطانی استخوان مورد مطالعه قرار گرفته است. به منظور بهینهسازی در فرایند دارورسانی به بافت هدف، فرمولاسیونهای مختلفی از نانوحامل نیوزومیحاوی عصاره طراحی شده است و پارامترهای مختلف این سامانهها از قبیل میزان بارگذاری عصاره، میزان و سرعت رهایش عصاره و همچنین میزان سمیت سلولی سامانه در مقابل سلول سرطانی مذکور مورد بررسی قرار گرفته است.
مواد و روشها
منابع گیاهی و عصارهگیری
گیاه پونهسای ایرانی در فصل گلدهی از ایستگاه تحقیقاتی گیاهان دارویی یزد جمعآوری شد و توسط بخش گیاهشناسی مرکز تحقیقات و آموزش کشاورزی و منابع طبیعی دانشگاه یزد مورد شناسایی قرار گرفت. این گونه در هرباریوم مرکز تحقیقات مذکور به شماره هرباریومی 3059 موجود است. گیاه در محیطی سایه و به دور از تابش مستقیم نور خورشید خشک شد. عصارهگیری از گیاه پونهسای ایرانی با استفاده از دستگاه سوکسله انجام پذیرفت. بدین منظور، گیاه خشکشده توسط دستگاه خردکن خانگی آسیاب شد، مقداری از آن جهت عصارهگیری داخل کارتوش بارگذاری شد و در داخل سیستم سوکسله قرار داده شد. از حلال اتانول 70 درصد نیز به عنوان حلال مناسب جهت عصارهگیری استفاده شد. عمل عصارهگیری طی پنج مرحله تکرار شد تا ترکیبات گیاه به طور کامل استخراج شود. بعد از اتمام عصارهگیری، محتویات بالن صاف شد و عصاره حاصل در داخل یک ظرف شیشهای روباز، در مجاورت هوا و به دور از تابش نور خورشید خشک شد. عصاره خشکشده جهت انجام آزمایشات بعدی مورد استفاده قرار گرفت.
تهیه و سنتزنانونیوزوم
از روش آبدهی فیلم نازک که روشی کلاسیک در تهیه وزیکولهاست برای سنتز نانونیوزومها استفاده شد. در این روش، فیلم نازک لیپیدی با تبخیرآمفیفیل درکلروفرم یا اتانول تشکیل میشود. بعد از تماس فیلم نازک با آب، نمونه حل میشود و فاز وزیکولی شکل میگیرد [12].
اختلاط فاز لیپیدی وتشکیل فیلم نازک
فاز لیپیدی شامل کلسترول-Span-60 (سیگما، آمریکا) است. در نمونه اصلی، فاز لیپیدی با چندین نسبت مولی متفاوت به کلروفرم (مرک، آلمان) اضافه و حل شد. اسانس به نسبت یک به 20 به فاز لیپدی اضافه شد. سپس فاز آلی محلول حاصل با استفاده از دستگاه تبخیرکننده دوار (هایدولف، آلمان) در دمای حدود 55 درجه سانتیگراد برای کلروفرم و با دور تقریبی 150 دور در دقیقه، حذف و فیلم نازک لیپیدی تشکیل شد. همچنین جهت اطمینان از حذف کامل حلّال، فیلم نازک لیپیدی چندین دقیقه با گاز نیتروژن هوادهی شد و 24 ساعت در دمای چهار درجه سانتیگراد قرار گرفت.
آبدهی فیلم لیپیدی
در این مرحله آب دیونیزه اضافه شد تا تا فیلم لیپیدی آبدهی شده و به همان غلظت اولیه میلیگرم بر میلیلیتر برسد. برای اختلاط بیشتر بدون روشن کردن خلأ 45 دقیقه تا یک ساعت بالن حاوی محلول فاز آبی به دستگاه تبخیرکننده دوار با دمای 37 درجه سانتیگراد و 150 دور بر دقیقه متصل شد، محلول شیریرنگ حاصل سوسپانسیون نیوزوم، حاوی عصاره است.
کاهش سایز
برای کاهش اندازه نیوزومهای چندلایه بزرگ و تشکیل وزیکولهای کوچک تکلایه از روش سونیکاسیون استفاده شد. پروب دستگاه سونیکاسیون در داخل محلول کلوئیدی نیوزومها قرارداده شد و سپس فرایند سونیکاسیون جهت تولید نیوزومهای تکجداره با توان 40 و 60 درصد (Amplitude) به مدت 10 دقیقه (10 ثانیه روشن و 15 ثانیه خاموش) انجام شد.
علاوه بر کاهش سایز به روش سونیکیت پروبی، میتوان از سونیکیت حمامی (Scientz، چین) نیز استفاده کرد که در این روش محلول کلوئیدی نیوزومها در سونیکیت حمامی قرار داده شده و دستگاه در دمای 37 درجه سانتیگراد نیم ساعت تنظیم میشود.
فرایند فیلتراسیون
قبل از فیلتراسیون، ناخالصی و مواد اضافی نمونهها (همچون تیتانیوم حاصل از سونیکاسیون پروبی) با استفاده از سانتریفیوژ با دور پنج هزار به مدت پنج دقیقه از محلول نیوزومی جداسازی شد. سپس به منظور جداسازی ذرات با اندازه بزرگتر از ذرات کوچکتر و همگن شدن محلول بهدستآمده در مرحله پیشفیلتراسیون از فیلتر 45/0 میکرومتر استفاده شد و در انتها جهت فیلتراسیون استریلکننده، محلول از فیلتر با قطر حفرات 22/0 میکرومتر عبور داده شد.
حذف عصاره آزاد Nepta
پس از بارگذاری عصاره به منظور جدا کردن عصاره بارگذارینشده، نیوزوم داخل کیسه دیالیز سلولزی ریخته شد و در بشر حاوی آب با حجم 150 برابر حجم نیوزوم به مدت دو ساعت در دمای چهار درجه سانتیگراد استیرر شد.
تعیین سایز و محدوده توزیع اندازه نانونیوزومهای حاوی عصاره
محدوده توزیع اندازه ذرات و همچنین پیک اندازه ذرات با استفاده از DLS و دستگاه نانوسایزر Brookhaven Instruments Corp تعیین شد. اندازهگیری نانونیوزومها در یک زاویه 90 درجه و تابش نور لیزر با طول موج 657 نانومتر در دمای 25 درجه سانتیگراد صورت گرفت. همچنین اندازهگیری نمونهها اغلب در پنج مرتبه و هر مرتبه با مدتزمان 30 ثانیه انجام شد. برای تهیه نمونه جهت تعیین اندازه به 600 میکرولیتر محلول با غلظت 5/0 - 1/0 میلیگرم بر میلیلیتر نیاز بود.
تعیین پتانسیل زتا نانونیوزوم
میزان بار سطحی و پتانسیل زتا نانونیوزومهای حامل عصاره با استفاده از دستگاه زتاسایزر شرکت Brookhaven Instruments Corp در دمای 25 درجه سانتیگراد اندازهگیری شد. برای تعیین بار سطحی به 1500 میکرولیتر محلول با غلظت 1/0 میلیگرم بر میلیلیتر نیاز است.
تصویربرداری از نانونیوزوم
از نانو نیوزومها با استفاده از میکروسکوپ الکترونیکی SEM به منظور بررسی شکل ظاهری و ساختار نانونیوزومهای تولیدی حامل عصاره تصویربرداری شد. یک قطره از نمونه با غلظت 1/0 میلیگرم بر میلیلیتر روی لامل ریخته شده شد. روی نمونه پس از خشک شدن، پوشش طلا داده شده و تصویر SEM تهیه شد.
آنالیز نانونیوزوم سنتزشده توسط دستگاه طیفسنجی مادون قرمز
گروههای عاملی سطح نانونیوزوم تولیدشده توسط آنالیز طیفسنجی مادون قرمز (FTIR) بررسی شد. در طیف FTIR عمدتاً دو ناحیه مورد توجه است. ناحیه گروه عاملی از cm-1 1550 تا 4000، ناحیهای است که بیشتر کششهای پیوندی اتفاق میافتد. در این ناحیه معمولاً تعداد نسبتاً کمی پیک وجود دارد. اما بسیاری از پیکهای آن مشخصکننده گروههای عاملی هستند. برای اطمینان از نبود عصاره آزاد و مواد اضافی در نمونه نانونیوزوم، از نمونه دیالیزشده نانونیوزومها، استفاده شد و به منظور کاهش رطوبت، حدود نیمساعت نمونه در آون با دمای تقریبی 60 درجه سانتیگراد قرار داده شد.
بررسی میزان بارگذاری عصاره داخل نیوزوم
به منظور بررسی میزان عصاره بارگذاریشده، نیوزومهای تهیهشده با نسبت یک به 9 با محلول ایزو 2 پروپانول (1 درصد وزنی به حجمی در آب) مخلوط شد و جذب آنها توسط دستگاه اسپکتروفوتومتر اندازه گرفته شد. نهایتاً غلظت عصاره با توجه به معادله نمودار کالیبراسیون و با استفاده از فرمول شماره 1 به دست آمد.

بررسی روند رهایش عصاره موجود در نیوزوم
برای بررسی رهایش عصاره، حجم مشخصی از نیوزوم حاوی آن داخل کیسه دیالیز سلولزی ریخته شد و در 10 سیسی بافر PBS قرار گرفت. نمونهگیری از آب در زمانهای 5/0، 1، 2، 3، 4، 5، 6، 7، 8، 24 و 48 ساعت و در دو دمای 37 و 48 درجه سانتیگراد انجام شد و جذب نمونهها توسط دستگاه اسپکتروفوتومتر مورد ارزیابی قرار گرفت.
بررسی سمیت سلولی نیوزومهای حاوی عصاره
در روش MTT به منظور تعیین سمیت سلولی نمونهها در برابر سلولهای سرطان استخوان انسان (MG-63) استفاده شد. در ابتدا تعداد مناسبی سلول (پنج هزار سلول در هر چاهک) در هریک از چاهکها کشت و اجازه داده شد تا سلولها به کف پلیت چسبیده و به حالت پایدار خود درآیند. سپس چاهکهای کنترل و آزمایش انتخاب شده و مقدار مناسبی از عصاره موردنظر، به چاهکهای تست اضافه شد و پلیت تا 48 ساعت جهت تأثیر ماده موردنظر، انکوبه شد. پس از اتمام زمان انکوباسیون محیط کشت رویی دور ریخته شده به هر چاهک 200 میکرولیتر محیط کشت حاوی نیم میلیگرم در میلیلیتر محلول MTT اضافه کرده، به مدت دو تا چهار ساعت در انکوباتور CO2 دار در دمای 37 درجه سانتیگراد قرار داده شد. در طی زمان انکوباسیون MTT، توسط سیستم سوکسینات دهیدروژناز که یکی از آنزیمهای چرخه تنفسی میتوکندریهاست، احیا میشود. احیا و شکسته شدن این حلقه موجب تولید کریستالهای آبیرنگ فورمازان میشود که در زیر میکروسکوپ بهراحتی قابل تشخیص هستند. میزان رنگ تولیدشده با تعداد سلولهایی که از نظر متابولیک فعال هستند رابطه مستقیم دارد. کریستالهای فورمازان در آب غیرمحلول بوده و بایستی قبل از رنگسنجی توسط ماده حلالی نظیر DMSO به حالت محلول درآیند. درنهایت جذب نوری محلول به دست آمده را میتوان در طول موج 570 نانومتر قرائت کرد و به کمک منحنی استاندارد، تعداد سلولها را محاسبه نمود [13].
آنالیز آماری دادهها
به منظور بررسی آماری نتایج، از نسخه 22 نرمافراز SPSS استفاده شد. جهت آنالیز آماری نتایج از تستهای آماری ANOVA و Student’s T-test استفاده شد و معناداری نتایج بر حسب 05/0>P سنجیده شد.
یافتهها
تعیین طول موج ماکسیمم عصاره N persica
طول موج 389 نانومتر به عنوان طول موج ماکسیمم عصاره هیدروالکلی استحصالشده که بیشترین میزان جذب را دارا بود، برای انجام آنالیزهای ثانویه انتخاب شد.
تولید نانونیوزوم حاوی عصاره Nepta
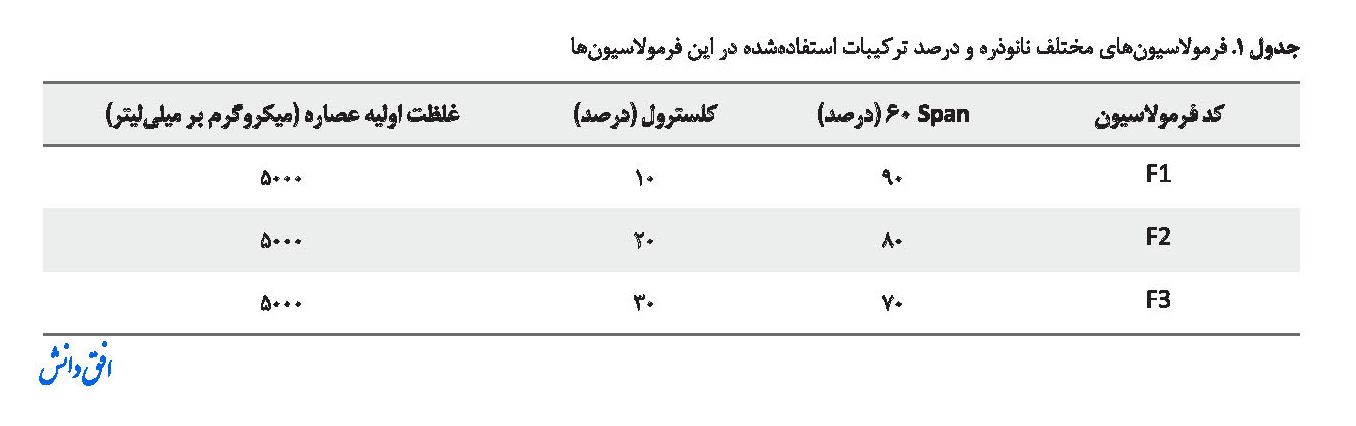
به منظور تهیه نانونیوزوم حاوی عصاره Nepta، سه فرمولاسیون مختلف (F1-F3) با استفاده از عصاره، کلسترول و Span-60 تهیه شد که دارای نسبتهای متفاوتی از ترکیبات بودند (جدول شماره 1).
برای بررسی رهایش عصاره، حجم مشخصی از نیوزوم حاوی آن داخل کیسه دیالیز سلولزی ریخته شد و در 10 سیسی بافر PBS قرار گرفت. نمونهگیری از آب در زمانهای 5/0، 1، 2، 3، 4، 5، 6، 7، 8، 24 و 48 ساعت و در دو دمای 37 و 48 درجه سانتیگراد انجام شد و جذب نمونهها توسط دستگاه اسپکتروفوتومتر مورد ارزیابی قرار گرفت.
بررسی سمیت سلولی نیوزومهای حاوی عصاره
در روش MTT به منظور تعیین سمیت سلولی نمونهها در برابر سلولهای سرطان استخوان انسان (MG-63) استفاده شد. در ابتدا تعداد مناسبی سلول (پنج هزار سلول در هر چاهک) در هریک از چاهکها کشت و اجازه داده شد تا سلولها به کف پلیت چسبیده و به حالت پایدار خود درآیند. سپس چاهکهای کنترل و آزمایش انتخاب شده و مقدار مناسبی از عصاره موردنظر، به چاهکهای تست اضافه شد و پلیت تا 48 ساعت جهت تأثیر ماده موردنظر، انکوبه شد. پس از اتمام زمان انکوباسیون محیط کشت رویی دور ریخته شده به هر چاهک 200 میکرولیتر محیط کشت حاوی نیم میلیگرم در میلیلیتر محلول MTT اضافه کرده، به مدت دو تا چهار ساعت در انکوباتور CO2 دار در دمای 37 درجه سانتیگراد قرار داده شد. در طی زمان انکوباسیون MTT، توسط سیستم سوکسینات دهیدروژناز که یکی از آنزیمهای چرخه تنفسی میتوکندریهاست، احیا میشود. احیا و شکسته شدن این حلقه موجب تولید کریستالهای آبیرنگ فورمازان میشود که در زیر میکروسکوپ بهراحتی قابل تشخیص هستند. میزان رنگ تولیدشده با تعداد سلولهایی که از نظر متابولیک فعال هستند رابطه مستقیم دارد. کریستالهای فورمازان در آب غیرمحلول بوده و بایستی قبل از رنگسنجی توسط ماده حلالی نظیر DMSO به حالت محلول درآیند. درنهایت جذب نوری محلول به دست آمده را میتوان در طول موج 570 نانومتر قرائت کرد و به کمک منحنی استاندارد، تعداد سلولها را محاسبه نمود [13].
آنالیز آماری دادهها
به منظور بررسی آماری نتایج، از نسخه 22 نرمافراز SPSS استفاده شد. جهت آنالیز آماری نتایج از تستهای آماری ANOVA و Student’s T-test استفاده شد و معناداری نتایج بر حسب 05/0>P سنجیده شد.
یافتهها
تعیین طول موج ماکسیمم عصاره N persica
طول موج 389 نانومتر به عنوان طول موج ماکسیمم عصاره هیدروالکلی استحصالشده که بیشترین میزان جذب را دارا بود، برای انجام آنالیزهای ثانویه انتخاب شد.
تولید نانونیوزوم حاوی عصاره Nepta
به منظور تهیه نانونیوزوم حاوی عصاره Nepta، سه فرمولاسیون مختلف (F1-F3) با استفاده از عصاره، کلسترول و Span-60 تهیه شد که دارای نسبتهای متفاوتی از ترکیبات بودند (جدول شماره 1).
با توجه به اینکه هدف از طراحی و بهینهسازی فرمولاسیون سنتزشده، بهبود میزان درونگیری عصاره در نانوحامل نیوزومی، است، این پارامتر به عنوان عامل مهم و تأثیرگذار در رفتار نانوحامل، مورد توجه و مقایسه قرار گرفت. با توجه به دادهها، فرمولاسیون F2 با 11/79 درصد بارگذاری، بیشترین میزان درونگیری عصاره را داشت. بنابراین، این فرمولاسیون به عنوان فرمولاسیون بهینه جهت بررسی پروفایل رهایش و آنالیزهای ساختاری و همچنین تستهای سلولی انتخاب شد.
بررسی الگوی رهایش نانوحامل نیوزومی
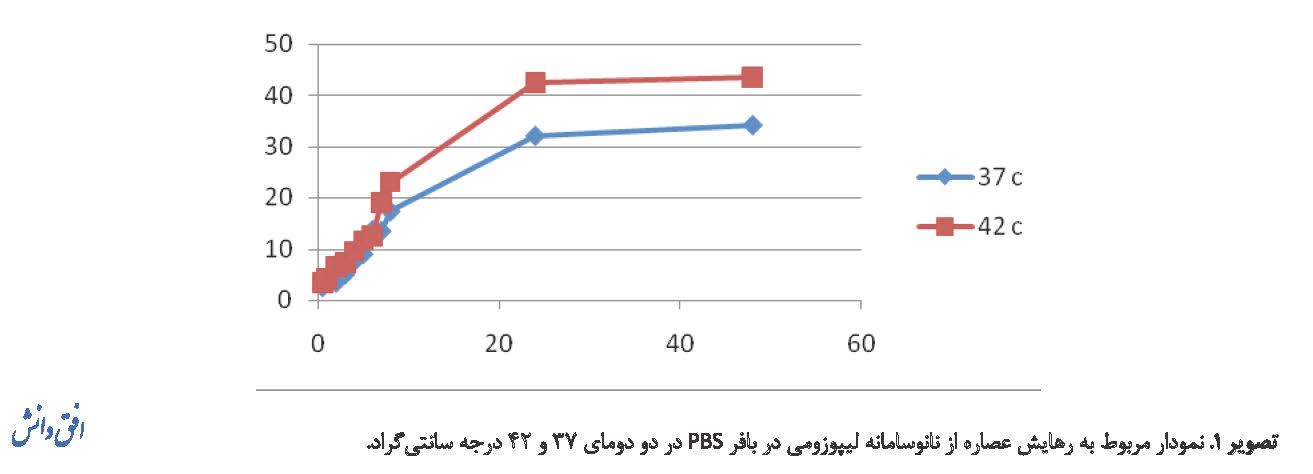
میزان آزادسازی عصاره از نانوحامل نیوزومی در دو شرایط دمایی 37 و 42 درجه، به ترتیب به عنوان دمای مناسب جهت رشد سلولهای سالم و سلولهای سرطانی اندازهگیری شد. بررسی نتایج حاصل نشان میدهد که در بازه زمانی پنج تا 10 ساعت اولیه، شیب نمودار تند بوده، آزادسازی عصاره با سرعت بالایی انجام میگیرد که با توجه به شیب غلظت ایجادشده در لحظه اول رهایش، دور از انتظار نیست. بررسی نتایج نشان میدهد سیر صعودی میزان رهایش تا زمان 24 ساعت ادامه داشته است و پس از آن میزان رهایش ثابت شده است که به منزله یکسان بودن شیب غلظتی بین سامانه و محیط پیرامون است. پس از این، نانوحامل با یک شیب تقریباً ثابت به روند آزادسازی ادامه میدهد که نشاندهنده پیوستگی رهایش است. با توجه به اینکه دمای سلولهای سرطانی 42 درجه است، دادهها نشان میدهد که رهایش در این دما بیشتر از سلولهای سالم است و میتواند ثابت کند که نانوحاملها دارای حساسیت به دما بوده و نیمههدفمند هستند. با توجه به دادهها، بازده رهاسازی 48ساعته عصاره در دمای 42 و 37 درجه به ترتیب 53/43 و 16/34 درصد است. دادههای حاصل از میزان رهایش نمونه در زمانهای مختلف و در دو دمای بررسیشده در تصویر شماره 1 نشان داده شده است. در مقایسه دو نمودار میتوان نتیجهگیری کرد که میزان رهایش در دمای 42 درجه سانتیگراد بالاتر از رهایش در دمای طبیعی بدن (37 درجه سانتیگراد) است که همین امر ثابت میکند که سامانه در تحویل عصاره در سایت هدف مؤثرتر رفتار کرده است و در اصطلاح گفته میشود که سامانه دارای شرایط نیمههدفمندی است.
میزان آزادسازی عصاره از نانوحامل نیوزومی در دو شرایط دمایی 37 و 42 درجه، به ترتیب به عنوان دمای مناسب جهت رشد سلولهای سالم و سلولهای سرطانی اندازهگیری شد. بررسی نتایج حاصل نشان میدهد که در بازه زمانی پنج تا 10 ساعت اولیه، شیب نمودار تند بوده، آزادسازی عصاره با سرعت بالایی انجام میگیرد که با توجه به شیب غلظت ایجادشده در لحظه اول رهایش، دور از انتظار نیست. بررسی نتایج نشان میدهد سیر صعودی میزان رهایش تا زمان 24 ساعت ادامه داشته است و پس از آن میزان رهایش ثابت شده است که به منزله یکسان بودن شیب غلظتی بین سامانه و محیط پیرامون است. پس از این، نانوحامل با یک شیب تقریباً ثابت به روند آزادسازی ادامه میدهد که نشاندهنده پیوستگی رهایش است. با توجه به اینکه دمای سلولهای سرطانی 42 درجه است، دادهها نشان میدهد که رهایش در این دما بیشتر از سلولهای سالم است و میتواند ثابت کند که نانوحاملها دارای حساسیت به دما بوده و نیمههدفمند هستند. با توجه به دادهها، بازده رهاسازی 48ساعته عصاره در دمای 42 و 37 درجه به ترتیب 53/43 و 16/34 درصد است. دادههای حاصل از میزان رهایش نمونه در زمانهای مختلف و در دو دمای بررسیشده در تصویر شماره 1 نشان داده شده است. در مقایسه دو نمودار میتوان نتیجهگیری کرد که میزان رهایش در دمای 42 درجه سانتیگراد بالاتر از رهایش در دمای طبیعی بدن (37 درجه سانتیگراد) است که همین امر ثابت میکند که سامانه در تحویل عصاره در سایت هدف مؤثرتر رفتار کرده است و در اصطلاح گفته میشود که سامانه دارای شرایط نیمههدفمندی است.
بررسی و مقایسه اندازه و بار سطحی نانوحامل نیوزومی حاوی عصاره
با توجه به اهمیت اندازه و بار سطحی نانوحامل در بسیاری از رفتارهای مطلوب آن، حامل نیوزومی از نقطهنظر اندازه و بار مورد آنالیز قرار میگیرد. اندازه نانو نیوزومهای تولیدی حاوی عصاره که به روش سونیکه کردن کاهش اندازه داده شدهاند به طور میانگین با استفاده از دستگاه نانوسایزر اندازهگیری شد. با توجه به نتایج گزارششده، اندازه نانوحامل نیوزومیحاوی عصاره 6/108 نانومتر تعیین شد.
پتانسیل زتای سطح نانو نیوزومهای تولیدی نیز با استفاده از دستگاه زتاسایزر اندازهگیری شد. میزان بار سطحی نانوحامل نیوزومیحاوی عصاره به طور میانگین 18/1±02/38- میلیولت به دست آمد.
با توجه به اهمیت اندازه و بار سطحی نانوحامل در بسیاری از رفتارهای مطلوب آن، حامل نیوزومی از نقطهنظر اندازه و بار مورد آنالیز قرار میگیرد. اندازه نانو نیوزومهای تولیدی حاوی عصاره که به روش سونیکه کردن کاهش اندازه داده شدهاند به طور میانگین با استفاده از دستگاه نانوسایزر اندازهگیری شد. با توجه به نتایج گزارششده، اندازه نانوحامل نیوزومیحاوی عصاره 6/108 نانومتر تعیین شد.
پتانسیل زتای سطح نانو نیوزومهای تولیدی نیز با استفاده از دستگاه زتاسایزر اندازهگیری شد. میزان بار سطحی نانوحامل نیوزومیحاوی عصاره به طور میانگین 18/1±02/38- میلیولت به دست آمد.
بررسی مورفولوژی نانوذرات نیوزومی
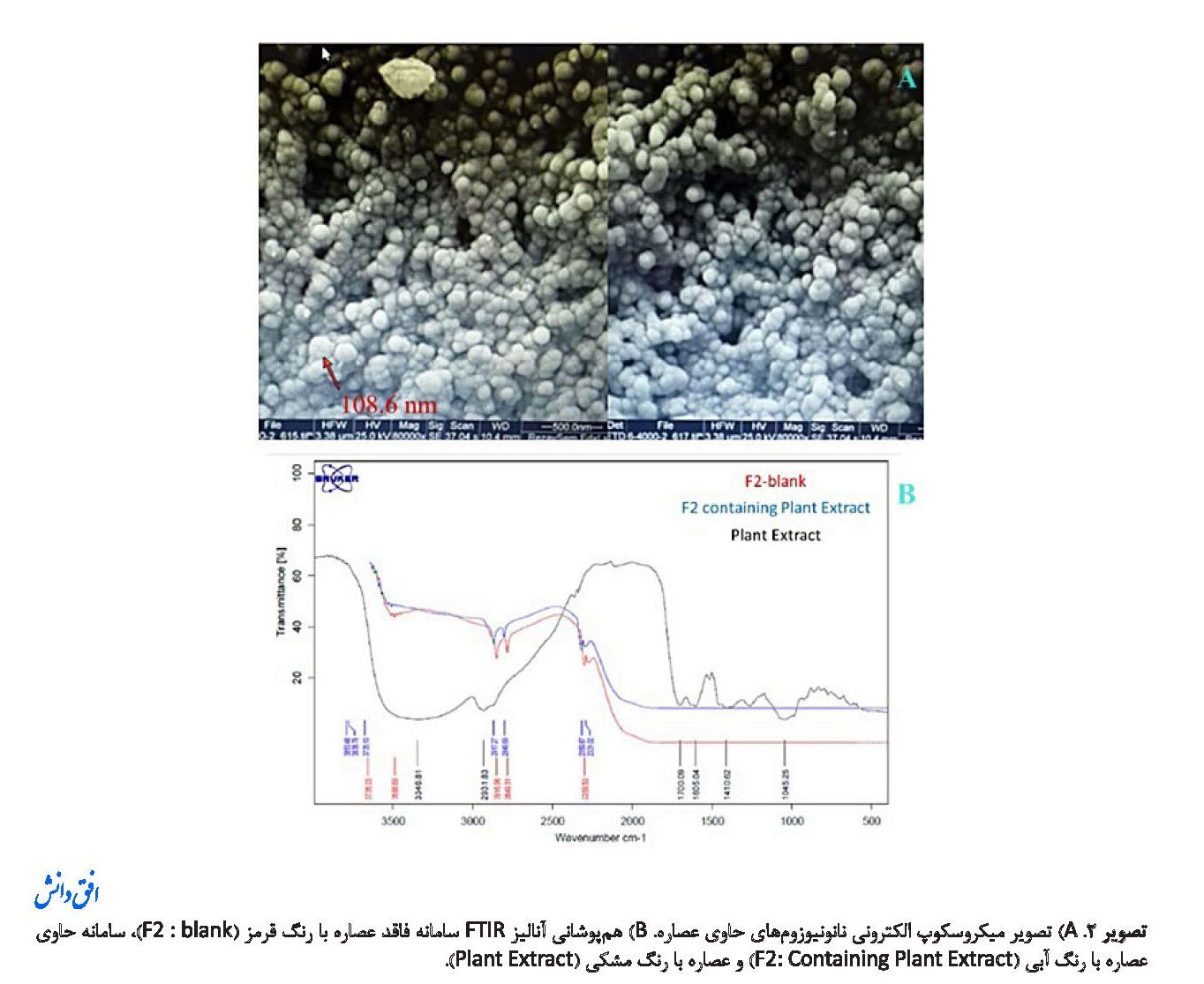
تصویر شماره A-2 مورفولوژی نانوذرات ساختهشده با استفاده از دستگاه میکروسکوپ الکترونی نمایه را نمایش میدهد. همانگونه که در تصویر مشخص است ذرات دارای توزیع اندازه مناسب و ساختارکرویشکل هستند که از مشخصات نانوحامل لیپیدی است و اثری از تجمع ناخواسته نانوذرات که نشاندهنده ناپایداری نانوذره است، دیده نمیشود.
بررسی پایداری نانوحامل حاوی عصاره
به منظور بررسی پایداری ساختاری نانوحامل تولیدشده، عدم برهمکنش شیمیایی عصاره و نانوحامل با استفاده از تکنیک FTIR مورد مطالعه قرار گرفت. بدین منظور ابتدا از عصاره، کلسترول و Span-60 که در ساخت نانوحامل مورد استفاده قرار گرفته بودند، به طور مجزا طیف FTIR گرفته شد و سپس با طیف FTIR سامانه تهیهشده مقایسه شد (تصویر شماره B-2). با توجه به طیفهای بهدستآمده چنین تحلیل میشود که در سامانه بدون حضور عصاره، پیک شاخص cm-1 3566 نشاندهنده گروه عاملی الکلی است که همین پیک با چند درجه اختلاف در سامانه حاوی عصاره به میزان cm-13500 تکرار شده است. پیک شاخص cm-1 2916 حضور گروه عاملی آلکانها با پیوند کششی C-H را نشان میدهد که در سامانه با عصاره دقیقاً همین عدد تکرار شده است. همچنین پیک cm-1 2849 نیز گروه عاملی هیدروکربنی با پیوند –CH2 را نشان میدهد که در سامانهای که عصاره در آن انکپسوله شده است، عیناً تکرار شده است. پیک شاخص cm-1 2359 نیز نشاندهنده گروه عاملی فسفین با پیوند کششی P-H است که در سامانه حاوی عصاره نیز تکرار شده است. تنها تفاوت در سامانه حاوی عصاره حضور پیک اضافه cm-1 2331 است که نشاندهنده گروه عاملی فسفین است که در سامانه تنها دیده نمیشود.
تصویر شماره A-2 مورفولوژی نانوذرات ساختهشده با استفاده از دستگاه میکروسکوپ الکترونی نمایه را نمایش میدهد. همانگونه که در تصویر مشخص است ذرات دارای توزیع اندازه مناسب و ساختارکرویشکل هستند که از مشخصات نانوحامل لیپیدی است و اثری از تجمع ناخواسته نانوذرات که نشاندهنده ناپایداری نانوذره است، دیده نمیشود.
بررسی پایداری نانوحامل حاوی عصاره
به منظور بررسی پایداری ساختاری نانوحامل تولیدشده، عدم برهمکنش شیمیایی عصاره و نانوحامل با استفاده از تکنیک FTIR مورد مطالعه قرار گرفت. بدین منظور ابتدا از عصاره، کلسترول و Span-60 که در ساخت نانوحامل مورد استفاده قرار گرفته بودند، به طور مجزا طیف FTIR گرفته شد و سپس با طیف FTIR سامانه تهیهشده مقایسه شد (تصویر شماره B-2). با توجه به طیفهای بهدستآمده چنین تحلیل میشود که در سامانه بدون حضور عصاره، پیک شاخص cm-1 3566 نشاندهنده گروه عاملی الکلی است که همین پیک با چند درجه اختلاف در سامانه حاوی عصاره به میزان cm-13500 تکرار شده است. پیک شاخص cm-1 2916 حضور گروه عاملی آلکانها با پیوند کششی C-H را نشان میدهد که در سامانه با عصاره دقیقاً همین عدد تکرار شده است. همچنین پیک cm-1 2849 نیز گروه عاملی هیدروکربنی با پیوند –CH2 را نشان میدهد که در سامانهای که عصاره در آن انکپسوله شده است، عیناً تکرار شده است. پیک شاخص cm-1 2359 نیز نشاندهنده گروه عاملی فسفین با پیوند کششی P-H است که در سامانه حاوی عصاره نیز تکرار شده است. تنها تفاوت در سامانه حاوی عصاره حضور پیک اضافه cm-1 2331 است که نشاندهنده گروه عاملی فسفین است که در سامانه تنها دیده نمیشود.
به طور کلی، با مقایسه طیف FTIR هر سه نمونه عصاره، سامانه حاوی عصاره و بدون آن، میتوان نتیجه گرفت که بسیاری از پیکهای شاخص معرفیکننده گروههای عاملی در عصاره، با کپسوله شدن آن در سامانه نیوزومیحذف شده است و چنین رخدادی نتیجه از دسترس خارج شدن گروههای عاملی عصاره با توجه به قرار گرفتن آن در سامانه است. همچنین حضور عصاره در سامانه سبب ایجاد هیچ پیک اضافه که نشان از ایجاد ساختار شیمیایی جدید و یا تجزیه ساختاری ترکیبات تشکیلدهنده سامانه باشد، نشده است. در نتیجه حضور عصاره هیچ برهمکنش شیمیایی ناخواستهای با سامانه برقرار نکرده است.
بررسی ورود نانو حامل نیوزومی به سلول سرطانی MG-63
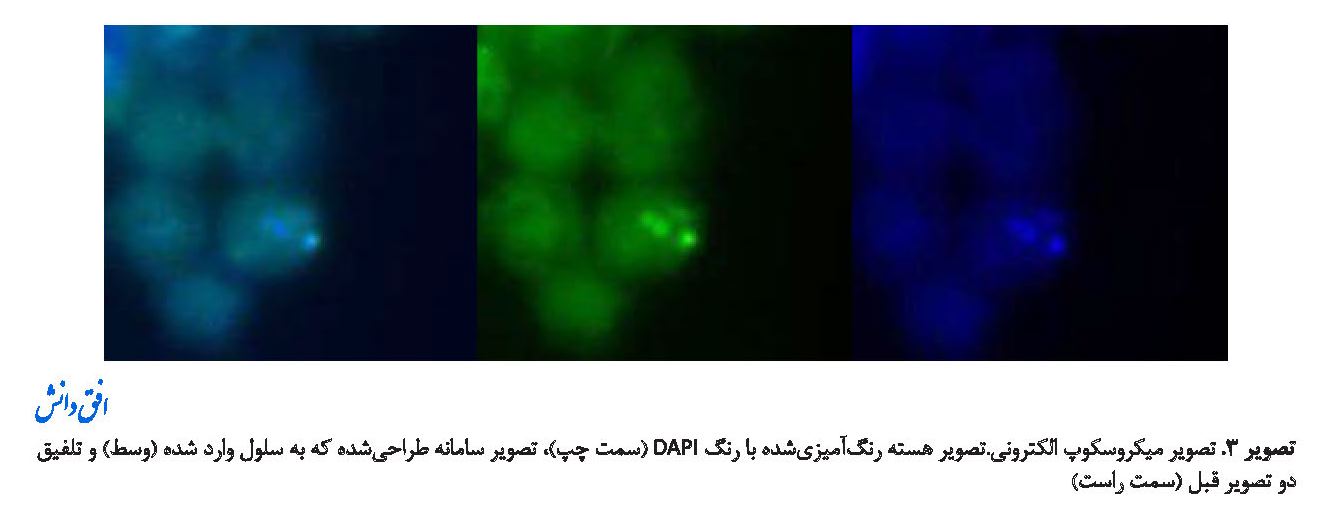
تصویر شماره 3، نحوه ورود عصاره به درون نانوحامل نیوزومی تولیدشده را نشان میدهد. طبق تصاویر میکروسکوپ الکترونی، بارگذاری عصاره در نانو حامل در حد قابل قبولی انجام شده است.
تصاویر گرفتهشده از میکروسکوپ فلورسنت، بهخوبی گواه بر ورود نانوسامانه به درون سلول و وقوع برداشت سلولی است (به ترتیب از چپ به راست)؛ هسته سلول رنگآمیزیشده با DAPI و استفاده از فیلتر آبی، سامانه نیوزومی رنگآمیزیشده با رنگ Dil و استفاده از فیلتر سبز. همپوشانی فیلترهای آبی و سبز نشان از ورود نانوسامانه به درون سلول دارد.
اندازهگیری اثر عصاره و نانوحامل بر میزان زندهمانی سلولهای MG-63
درصد زندهمانی سلولهای سرطانی مغز استخوان (MG-63) در برابر غلظت 100 میکروگرم بر میلیلیتر از هر کدام از نمونههای نیوزوم فاقد عصاره، عصاره آزاد و نیوزوم حاوی عصاره، پس از 48 ساعت تیمار، با استفاده از تست MTT مورد بررسی قرار گرفت (تصویر شماره 4). نتایج حاصل از آزمون MTT نیوزوم فاقد عصاره نشان از سمیت ناچیز سامانه خالی داشت. میزان زندهمانی سلولهای سرطانی در مقابل این نمونه 16/92 درصد محاسبه شد. مقایسه میزان زندهمانی سلولهای MG-63 در مقابل مقادیر یکسان از فرم آزاد عصاره Nepeta persica و سامانه نیوزومیحاوی آن، نشان از عملکرد بهتر سامانه نیوزومیداشت. میزان زندهمانی سلولها در مقابل این دو نمونه، به ترتیب 22 و 88/5 درصد به دست آمد و به معنی این است که در غلظتهای یکسان، سامانه نیوزومی درصد بیشتری از سلولهای سرطانی را از بین میبرد. این امر نشان از اثرگذاری بیشتر عصاره درون نانوحامل نیوزومی دارد؛ بدانگونه که توانسته است در مقایسه با عصاره آزاد برداشت سلولی بیشتری داشته باشد و سمیت سلولی بالاتری را القا کند. تصویر شماره 4 که نشاندهنده نتایج آزمون MTT است، درواقع رسالت نانوسامانه را بهخوبی در معرض نمایش قرار داده است. این موضوع با توجه به نانومقیاس بودن حامل و تسهیل در ورود عصاره به درون سلولهای MG-63 توجیهپذیر است.
بررسی معنیداری و یا عدم معنیداری دادههای حاصل از آزمون MTT، با استفاده از نرمافزار SPSS انجام پذیرفت. معیار معنیداری مقدار P کوچکتر از 05/0 و یا به اصطلاح پنج درصد در نظر گرفته شد.
بر اساس نتایج حاصل از آنالیز آماری دادههای حاصل از MTT، اختلافات در میزان بقای سلولها پس از قرارگیری در معرض سه تیمار عصاره آزاد، نیوزوم فاقد عصاره و نیوزوم حاوی عصاره کاملاً معنیدار است و نشاندهنده عدم تصادفی بودن آنهاست (P<0/05).
شیوههای مرسوم جهت درمان سرطان، بر ریشهکن کردن سلولهای توموری، از طریق شیمیدرمانی و رادیوتراپی و فعالسازی سیستم ایمنی برای از بین بردن سلولهای توموری تأکید دارد. با اینکه این شیوههای درمانی در برخی از سرطانها پاسخ خوبی داشته است، لازم است درمانهای اختصاصیتری برای بیمارانی که به درمانهای معمول پاسخ نمیدهند، ابداع شود. روشهای مختلفی برای کاهش عوارض جانبی و افزایش بازده درمان به کار گرفته شده است. امروزه، محققان رشته داروسازی سعی بر جایگزین کردن گیاهان دارویی و ترکیبات مؤثر آنها به جای داروهای شیمیایی دارند که گاه عوارض جانبی جبرانناپذیری را به بیمار وارد میکنند [14].
در مطالعه اخیر، سه سامانه نانونیوزومی مختلف با استفاده از نسبتهای متفاوت از دو ترکیب کلسترول و Span-60 که هر سه حاوی مقدار یکسانی از عصاره گیاه پونهسای ایرانی (پنج میلیگرم بر میلیلیتر) بودند، طراحی و سنتز شد. به منظور مشخص کردن مناسبترین فرمولاسیون، آزمونهای مختلفی روی سامانههای حاصله انجام شد که نهایتاً سامانه تولیدی با 80 درصد Span-60 و 20 درصد کلسترول به عنوان فرمولاسیون برتر شناسایی شد. خاصیت سمیت سلولی عصاره آزاد و عصاره محصور در این فرمولاسیون نیز از طریق تست MTT مورد آنالیز واقع شد. درصد زندهمانی سلولهای سرطانی مغز استخوان در برابر غلظت 100 میکروگرم بر میلیلیتر از عصاره، 22 درصد به دست آمد که نشان از خاصیت ضدسرطانی عصاره گیاه پونهسای ایرانی است. خلیقی سیگارودی و همکاران در سال 2013 ترکیبهای شیمیایی عصاره و فعالیت آنتیاکسیدانی گونه Nepeta pogonosperma را بررسی کردند و ترکیبهای فنلی را گزارش کردند و به این نتیجه رسیدند که این گیاه دارای اثرات آنتیاکسیدانی است و احتمال میرود خواص آنتیاکسیدانی بیشتر در گیاهانی موجود باشند که حاوی ترکیبات فنلی هستند [15]. در سال 2014 ابوالفضل شاکری و همکاران ترکیب های شیمیایی و فعالیت آنتیباکتریال و سمیت سلولی Nepeta ucrainica را بررسی کردند و به این نتیجه رسیدند که عصاره این گیاه دارای فعالیت آنتیباکتریال بهخصوص در برابر باکتریهای گرم مثبت است و همچنین سبب مهار رشد رده سلولی سرطان تخمدان و سرطان پستان شدند و فعالیت سایتوتوکسیک وابسته به دُز قابل توجهی در مقابل MCF-7 و A2780 است [16].
از دیگر روشهایی که بهشدت مورد توجه محققین در زمینه درمان سرطان است، دارورسانی هدفمند به بافت هدف است که در نتیجه آن، اثربخشی دارو افزایش یافته و سمیت دارویی کاهش مییابد. در این راستا، صنعت داروسازی نوین اقدام به تولید و استفاده از سیستمهای نوین دارورسانی کرد. از مهمترین این سیستمها که امروزه تحقیقات گستردهای روی آنها انجام میشود، میتوان به هیدروژلها، نانوفیبرها، نانولیپوزومها، نیوزومها و نانودرختسان اشاره کرد [18 ،17].
در تحقیق حاضر، مقایسه تأثیر سمیت سلولی نیوزوم حاوی عصاره Nepeta persica با فرم آزاد عصاره نشان داد که القای مرگ سلولی در حضور عصاره N. persica بهتنهایی و فرم نیوزومه عصاره N. persica (غلظت های یکسان عصاره سلولی) متفاوت است؛ به طوری که درصد زنده ماندن سلولهای سرطانی در حضور فرم نیوزومه عصاره کمتر از فرم عصاره تنهاست. در مطالعات مشابهی، Fang و همکاران در سال 2001 اثر نیوزومها و لیپوزومها را در نفوذپذیری پوستی داروی enoxacin مشاهده کردند. آنها همچنین مشاهده کردند که گنجاندن کلسترول در enoxacin باعث بهبود ثبات دارو میشود [19]. Mujoriya و همکاران روی طراحی و تولید سیستم تحویل نیوزومی برای کتوپروفن کار کردند. آنها به این نتیجه رسیدند که دارورسانی هدفمند به بافت هدف، اثر درمانی داروی کیتوپروفن را افزایش میدهد و باعث کاهش اثرات نامطلوب آن روی بافتهای غیرهدف میشود. در نتایج تحقیق Mujoriya و تیم وی، وزیکولهای نیوزومی حاوی کیتوپروفن به عنوان یک سیستم رهایش بسیار مطلوب عمل کردند [20]. در مطالعهای دیگر Srinivas و همکاران در سال 2010 روی تهیه و ارزیابی نیوزومهای حاوی آسیکلوفناک، مشخص شد آسیکلوفناک دارویی است که دارای خواص درمانی ضعیف و نیمه عمر زیستی کوتاه است. هدف آنها از این مطالعه تولید و بهینهسازی فرمولاسیونی از آسیکلوفناک به منظور بهتر کردن زیست دسترسی آن بود. در این مطالعه اثر ترکیبات مختلف مانند سورفکتانتهای غیریونی و کلسترول بر روی بازده کپسولاسیون، اندازه ذرات و آزادسازی یا رهایش دارو مورد ارزیابی قرار گرفت. آنها به این نتیجه رسیدند که در حضور این نوع از سورفاکتانتها، میزان رهایش دارو در تمام فرمولاسیونها افزایش مییابد، همچنین با افزایش غلظت سورفکتانت، بازده به دام انداختن دارو نیز افزایش نشان میدهد [21]. عسکری و همکاران در سال 2019 اثر سمیت سلولی عصاره پوست انار را به فرم نیوزومه بر سرطان پستان بررسی کردند و نشان دادند استفاده از نیوزوم به عنوان حامل باعث رسانش بهتر عصاره شده و میزان بقا را بیشتر کاهش میدهد. در ضمن میزان رهایش و اثرگذاری عصاره از نانوحامل در شرایط سلولهای سرطانی (از نظر دما و pH) بهتر است که مجموعه یافتههای آنها مشابه نتایج این مطالعه است [22]. کریمی مقدم و همکاران نیز در سال 2019 جهت رسانش داروی سیلیبینین به سلولهای سرطان پستان از نیوزوم به عنوان حامل استفاده کردند و در یافتههایی مشابه نتایج این مطالعه، اثرگذاری بیشتر فرم نیوزومه داروی سیلیبینین را نسبت فرم آزاد دارو مشاهده کردند [23]. همچنین بهرامی بنان و همکاران در سال 2018 و پرداختی و همکاران در سال 2012 نیز مطابق با یافتههای این مقاله، نشان دادند که میزان انتقال، عملکرد و تأثیرگذاری دارو و حتی واکسن در شرایط کپسولهشده نسبت به شرایط غیرکپسوله بیشتر است [25 ،24]. در پژوهش صورتگرفته نیز نانونیوزوم طراحیشده باعث بهبود خاصیت سمیت سلولی عصاره گیاه پونهسای ایرانی و رهایش آهسته و پیوسته دارو به مدت طولانیتر شد که مناسب درمان بیماری سرطان است.
بحث و نتیجهگیری
استفاده از علم نانوتکنولوژی در زمینه پزشکی و داروسازی توانسته پنجره امیدی در درمان بیماریهای صعبالعلاج به روی محققین باز کند و نانولیپوزومها و نانونیوزومها توانستهاند بخش وسیعی از تحقیقات را به خود اختصاص دهند. نتایج این مطالعه نشان از اثربخشی بهتر و مناسبتر فرم نانونیوزومی عصاره گیاه پونهسای ایرانی نسبت به فرم آزاد عصاره در توانایی ورود به سلول و القای اثرات ضدسرطانی داشت.
ملاحظات اخلاقی
پیروی از اصول اخلاق پژوهش
این پژوهش بر اساس اصول اخلاقی حفاظت از آزمودنیهای انسانی انجام گرفته و از نظر اخلاق زیستی طی نامه شماره 98975 مورد تأیید کمیته اخلاق در پزشکی دانشگاه آزاد اسلامی است.
حامی مالی
این مقاله حامی مالی ندارد.
مشارکت نویسندگان
تمام نویسندگان در طراحی، اجرا و نگارش همه بخشهای پژوهش حاضر مشارکت داشتهاند.
تعارض منافع
هیچگونه تعارض منافعی توسط نویسندگان بیان نشده است.
تشکر و قدردانی
نویسندگان مراتب قدردانی خود را از دانشکده پیراپزشکی دانشگاه علومپزشکی شهید صدوقی یزد اعلام میدارند.
بررسی ورود نانو حامل نیوزومی به سلول سرطانی MG-63
تصویر شماره 3، نحوه ورود عصاره به درون نانوحامل نیوزومی تولیدشده را نشان میدهد. طبق تصاویر میکروسکوپ الکترونی، بارگذاری عصاره در نانو حامل در حد قابل قبولی انجام شده است.
تصاویر گرفتهشده از میکروسکوپ فلورسنت، بهخوبی گواه بر ورود نانوسامانه به درون سلول و وقوع برداشت سلولی است (به ترتیب از چپ به راست)؛ هسته سلول رنگآمیزیشده با DAPI و استفاده از فیلتر آبی، سامانه نیوزومی رنگآمیزیشده با رنگ Dil و استفاده از فیلتر سبز. همپوشانی فیلترهای آبی و سبز نشان از ورود نانوسامانه به درون سلول دارد.
اندازهگیری اثر عصاره و نانوحامل بر میزان زندهمانی سلولهای MG-63
درصد زندهمانی سلولهای سرطانی مغز استخوان (MG-63) در برابر غلظت 100 میکروگرم بر میلیلیتر از هر کدام از نمونههای نیوزوم فاقد عصاره، عصاره آزاد و نیوزوم حاوی عصاره، پس از 48 ساعت تیمار، با استفاده از تست MTT مورد بررسی قرار گرفت (تصویر شماره 4). نتایج حاصل از آزمون MTT نیوزوم فاقد عصاره نشان از سمیت ناچیز سامانه خالی داشت. میزان زندهمانی سلولهای سرطانی در مقابل این نمونه 16/92 درصد محاسبه شد. مقایسه میزان زندهمانی سلولهای MG-63 در مقابل مقادیر یکسان از فرم آزاد عصاره Nepeta persica و سامانه نیوزومیحاوی آن، نشان از عملکرد بهتر سامانه نیوزومیداشت. میزان زندهمانی سلولها در مقابل این دو نمونه، به ترتیب 22 و 88/5 درصد به دست آمد و به معنی این است که در غلظتهای یکسان، سامانه نیوزومی درصد بیشتری از سلولهای سرطانی را از بین میبرد. این امر نشان از اثرگذاری بیشتر عصاره درون نانوحامل نیوزومی دارد؛ بدانگونه که توانسته است در مقایسه با عصاره آزاد برداشت سلولی بیشتری داشته باشد و سمیت سلولی بالاتری را القا کند. تصویر شماره 4 که نشاندهنده نتایج آزمون MTT است، درواقع رسالت نانوسامانه را بهخوبی در معرض نمایش قرار داده است. این موضوع با توجه به نانومقیاس بودن حامل و تسهیل در ورود عصاره به درون سلولهای MG-63 توجیهپذیر است.
بررسی معنیداری و یا عدم معنیداری دادههای حاصل از آزمون MTT، با استفاده از نرمافزار SPSS انجام پذیرفت. معیار معنیداری مقدار P کوچکتر از 05/0 و یا به اصطلاح پنج درصد در نظر گرفته شد.
بر اساس نتایج حاصل از آنالیز آماری دادههای حاصل از MTT، اختلافات در میزان بقای سلولها پس از قرارگیری در معرض سه تیمار عصاره آزاد، نیوزوم فاقد عصاره و نیوزوم حاوی عصاره کاملاً معنیدار است و نشاندهنده عدم تصادفی بودن آنهاست (P<0/05).
شیوههای مرسوم جهت درمان سرطان، بر ریشهکن کردن سلولهای توموری، از طریق شیمیدرمانی و رادیوتراپی و فعالسازی سیستم ایمنی برای از بین بردن سلولهای توموری تأکید دارد. با اینکه این شیوههای درمانی در برخی از سرطانها پاسخ خوبی داشته است، لازم است درمانهای اختصاصیتری برای بیمارانی که به درمانهای معمول پاسخ نمیدهند، ابداع شود. روشهای مختلفی برای کاهش عوارض جانبی و افزایش بازده درمان به کار گرفته شده است. امروزه، محققان رشته داروسازی سعی بر جایگزین کردن گیاهان دارویی و ترکیبات مؤثر آنها به جای داروهای شیمیایی دارند که گاه عوارض جانبی جبرانناپذیری را به بیمار وارد میکنند [14].
در مطالعه اخیر، سه سامانه نانونیوزومی مختلف با استفاده از نسبتهای متفاوت از دو ترکیب کلسترول و Span-60 که هر سه حاوی مقدار یکسانی از عصاره گیاه پونهسای ایرانی (پنج میلیگرم بر میلیلیتر) بودند، طراحی و سنتز شد. به منظور مشخص کردن مناسبترین فرمولاسیون، آزمونهای مختلفی روی سامانههای حاصله انجام شد که نهایتاً سامانه تولیدی با 80 درصد Span-60 و 20 درصد کلسترول به عنوان فرمولاسیون برتر شناسایی شد. خاصیت سمیت سلولی عصاره آزاد و عصاره محصور در این فرمولاسیون نیز از طریق تست MTT مورد آنالیز واقع شد. درصد زندهمانی سلولهای سرطانی مغز استخوان در برابر غلظت 100 میکروگرم بر میلیلیتر از عصاره، 22 درصد به دست آمد که نشان از خاصیت ضدسرطانی عصاره گیاه پونهسای ایرانی است. خلیقی سیگارودی و همکاران در سال 2013 ترکیبهای شیمیایی عصاره و فعالیت آنتیاکسیدانی گونه Nepeta pogonosperma را بررسی کردند و ترکیبهای فنلی را گزارش کردند و به این نتیجه رسیدند که این گیاه دارای اثرات آنتیاکسیدانی است و احتمال میرود خواص آنتیاکسیدانی بیشتر در گیاهانی موجود باشند که حاوی ترکیبات فنلی هستند [15]. در سال 2014 ابوالفضل شاکری و همکاران ترکیب های شیمیایی و فعالیت آنتیباکتریال و سمیت سلولی Nepeta ucrainica را بررسی کردند و به این نتیجه رسیدند که عصاره این گیاه دارای فعالیت آنتیباکتریال بهخصوص در برابر باکتریهای گرم مثبت است و همچنین سبب مهار رشد رده سلولی سرطان تخمدان و سرطان پستان شدند و فعالیت سایتوتوکسیک وابسته به دُز قابل توجهی در مقابل MCF-7 و A2780 است [16].
از دیگر روشهایی که بهشدت مورد توجه محققین در زمینه درمان سرطان است، دارورسانی هدفمند به بافت هدف است که در نتیجه آن، اثربخشی دارو افزایش یافته و سمیت دارویی کاهش مییابد. در این راستا، صنعت داروسازی نوین اقدام به تولید و استفاده از سیستمهای نوین دارورسانی کرد. از مهمترین این سیستمها که امروزه تحقیقات گستردهای روی آنها انجام میشود، میتوان به هیدروژلها، نانوفیبرها، نانولیپوزومها، نیوزومها و نانودرختسان اشاره کرد [18 ،17].
در تحقیق حاضر، مقایسه تأثیر سمیت سلولی نیوزوم حاوی عصاره Nepeta persica با فرم آزاد عصاره نشان داد که القای مرگ سلولی در حضور عصاره N. persica بهتنهایی و فرم نیوزومه عصاره N. persica (غلظت های یکسان عصاره سلولی) متفاوت است؛ به طوری که درصد زنده ماندن سلولهای سرطانی در حضور فرم نیوزومه عصاره کمتر از فرم عصاره تنهاست. در مطالعات مشابهی، Fang و همکاران در سال 2001 اثر نیوزومها و لیپوزومها را در نفوذپذیری پوستی داروی enoxacin مشاهده کردند. آنها همچنین مشاهده کردند که گنجاندن کلسترول در enoxacin باعث بهبود ثبات دارو میشود [19]. Mujoriya و همکاران روی طراحی و تولید سیستم تحویل نیوزومی برای کتوپروفن کار کردند. آنها به این نتیجه رسیدند که دارورسانی هدفمند به بافت هدف، اثر درمانی داروی کیتوپروفن را افزایش میدهد و باعث کاهش اثرات نامطلوب آن روی بافتهای غیرهدف میشود. در نتایج تحقیق Mujoriya و تیم وی، وزیکولهای نیوزومی حاوی کیتوپروفن به عنوان یک سیستم رهایش بسیار مطلوب عمل کردند [20]. در مطالعهای دیگر Srinivas و همکاران در سال 2010 روی تهیه و ارزیابی نیوزومهای حاوی آسیکلوفناک، مشخص شد آسیکلوفناک دارویی است که دارای خواص درمانی ضعیف و نیمه عمر زیستی کوتاه است. هدف آنها از این مطالعه تولید و بهینهسازی فرمولاسیونی از آسیکلوفناک به منظور بهتر کردن زیست دسترسی آن بود. در این مطالعه اثر ترکیبات مختلف مانند سورفکتانتهای غیریونی و کلسترول بر روی بازده کپسولاسیون، اندازه ذرات و آزادسازی یا رهایش دارو مورد ارزیابی قرار گرفت. آنها به این نتیجه رسیدند که در حضور این نوع از سورفاکتانتها، میزان رهایش دارو در تمام فرمولاسیونها افزایش مییابد، همچنین با افزایش غلظت سورفکتانت، بازده به دام انداختن دارو نیز افزایش نشان میدهد [21]. عسکری و همکاران در سال 2019 اثر سمیت سلولی عصاره پوست انار را به فرم نیوزومه بر سرطان پستان بررسی کردند و نشان دادند استفاده از نیوزوم به عنوان حامل باعث رسانش بهتر عصاره شده و میزان بقا را بیشتر کاهش میدهد. در ضمن میزان رهایش و اثرگذاری عصاره از نانوحامل در شرایط سلولهای سرطانی (از نظر دما و pH) بهتر است که مجموعه یافتههای آنها مشابه نتایج این مطالعه است [22]. کریمی مقدم و همکاران نیز در سال 2019 جهت رسانش داروی سیلیبینین به سلولهای سرطان پستان از نیوزوم به عنوان حامل استفاده کردند و در یافتههایی مشابه نتایج این مطالعه، اثرگذاری بیشتر فرم نیوزومه داروی سیلیبینین را نسبت فرم آزاد دارو مشاهده کردند [23]. همچنین بهرامی بنان و همکاران در سال 2018 و پرداختی و همکاران در سال 2012 نیز مطابق با یافتههای این مقاله، نشان دادند که میزان انتقال، عملکرد و تأثیرگذاری دارو و حتی واکسن در شرایط کپسولهشده نسبت به شرایط غیرکپسوله بیشتر است [25 ،24]. در پژوهش صورتگرفته نیز نانونیوزوم طراحیشده باعث بهبود خاصیت سمیت سلولی عصاره گیاه پونهسای ایرانی و رهایش آهسته و پیوسته دارو به مدت طولانیتر شد که مناسب درمان بیماری سرطان است.
بحث و نتیجهگیری
استفاده از علم نانوتکنولوژی در زمینه پزشکی و داروسازی توانسته پنجره امیدی در درمان بیماریهای صعبالعلاج به روی محققین باز کند و نانولیپوزومها و نانونیوزومها توانستهاند بخش وسیعی از تحقیقات را به خود اختصاص دهند. نتایج این مطالعه نشان از اثربخشی بهتر و مناسبتر فرم نانونیوزومی عصاره گیاه پونهسای ایرانی نسبت به فرم آزاد عصاره در توانایی ورود به سلول و القای اثرات ضدسرطانی داشت.
ملاحظات اخلاقی
پیروی از اصول اخلاق پژوهش
این پژوهش بر اساس اصول اخلاقی حفاظت از آزمودنیهای انسانی انجام گرفته و از نظر اخلاق زیستی طی نامه شماره 98975 مورد تأیید کمیته اخلاق در پزشکی دانشگاه آزاد اسلامی است.
حامی مالی
این مقاله حامی مالی ندارد.
مشارکت نویسندگان
تمام نویسندگان در طراحی، اجرا و نگارش همه بخشهای پژوهش حاضر مشارکت داشتهاند.
تعارض منافع
هیچگونه تعارض منافعی توسط نویسندگان بیان نشده است.
تشکر و قدردانی
نویسندگان مراتب قدردانی خود را از دانشکده پیراپزشکی دانشگاه علومپزشکی شهید صدوقی یزد اعلام میدارند.
References
Hart BL. The evolution of herbal medicine: Behavioural perspectives. Animal Behaviour. 2005; 70(5):975-89. [DOI:10.1016/j.anbehav.2005.03.005]
Geller DS, Gorlick R. Osteosarcoma: A review of diagnosis, management, and treatment strategies. Clinical Advances in Hematology & Oncology. 2010; 8(10):705-18. [PMID]
Moghassemi S, Hadjizadeh A. Nano-niosomes as nanoscale drug delivery systems: An illustrated review. Journal of Controlled Release. 2014; 185:22-36. [DOI:10.1016/j.jconrel.2014.04.015] [PMID]
Yang XB, Wu WY, Long SQ, Deng H, Pan ZQ. Effect of gefitinib plus Chinese Herbal Medicine (CHM) in patients with advanced non-small-cell lung cancer: A retrospective case-control study. Complementary Therapies in Medicine. 2014; 22(6):1010-8. [DOI:10.1016/j.ctim.2014.10.001] [PMID]
Cragg GM, Newman DJ. Plants as a source of anti-cancer agents. Journal of Ethnopharmacology. 2005; 100(1-2):72-9. [DOI:10.1016/j.jep.2005.05.011] [PMID]
Nobili S, Lippi D, Witort E, Donnini M, Bausi L, Mini E, et al. Natural compounds for cancer treatment and prevention. Pharmacological Research. 2009; 59(6):365-78. [DOI:10.1016/j.phrs.2009.01.017] [PMID]
Evans WC, Evans D, Trease GE. Trease and Evans pharmacognosy. Philadelphia: Saunders/Elsevier; 2009. https://books.google.com/books?id=ujetPwAACAAJ&dq
Baser KHC, Oözek T, Yildiz B, Bahçecioglu Z, Tuümen G. Composition of the essential oil of Nepeta fissa C.A.Meyer. Journal of Essential Oil Research. 2000; 12(1):27-8. [DOI:10.1080/10412905.2000.9712033]
Rapisarda A, Galati EM, Tzakou O, Flores M, Miceli N. Nepeta sibthorpii Bentham (Lamiaceae): Micromorphological analysis of leaves and flowers. Il Farmaco. 2001; 56(5-7):413-5. [DOI:10.1016/S0014-827X(01)01050-3]
Tzakou O, Harvala C, Galati EM, Sanogo R. Essential oil composition of Nepeta argolica Bory et Chaub. subsp. argolica. Flavour and Fragrance Journal. 2000; 15(2):115-8. [DOI:10.1002/(SICI)1099-1026(200003/04)15:2<115::AID-FFJ877>3.0.CO;2-9]
Mozaffarian V. [A dictionary of Iranian plant, names: Latin, English, Persian (Latin-English-Persian)]. 2nd ed. Tehran: Farhang Moaser; 1998. http://opac.nlai.ir/opac-prod/bibliographic/555105
Haghiralsadat F, Amoabediny G, Sheikhha MH, Zandieh-Doulabi B, Naderinezhad S, Helder MN, et al. New liposomal doxorubicin nanoformulation for osteosarcoma: Drug release kinetic study based on thermo and pH sensitivity. Chemical Biology & Drug Design. 2017; 90(3):368-79. [DOI:10.1111/cbdd.12953] [PMID]
Mosmann T. Rapid colorimetric assay for cellular growth and survival: Application to proliferation and cytotoxicity assays. Journal of Immunological Methods. 1983; 65(1-2):55-63. [DOI:10.1016/0022-1759(83)90303-4]
Zarei M, Arjmand M, Mohammadi M, Chiani M, Ebrahimi H, Akbarzadeh Khiavi A. [Preparation of nanoniosomal Paclitaxel formulation and survey of its cytotoxic effect on breast cancer cell line (MCF-7) (Persian)]. New Cellular & Molecular Biotechnology Journal. 2013; 3(12):17-23. http://ncmbjpiau.ir/article-1-438-en.pdf
Khalighi-Sigaroodi F, Ahvazi M, Ebrahimzadeh H, Rahimifard N. [Chemical composition of the essential oil and antioxidant activities, total phenol and flavonoid content of the extract of Nepeta pogonosperma (Persian)]. Journal of Medicinal Plants. 2013; 4(48):185-98. http://jmp.ir/article-1-72-en.html
Shakeri A, Khakdan F, Soheili V, Sahebkar AH, Rassam GA, Asili J. Chemical composition, antibacterial activity, and cytotoxicity of essential oil from Nepeta ucrainica L. spp. kopetdaghensis. Industrial Crops and Products. 2014; 58:315-21. [DOI:10.1016/j.indcrop.2014.04.009]
Moghimipour E, Kouchak M, Bahmandar R. [Nano-liposomes as new drug delivery carriers (Persian)]. Jundishapur Scientific Medical Journal. 2013; 12(5):467-83. http://jsmj.ajums.ac.ir/article_49795_en.html
Tiwari G, Tiwari R, Sriwastawa B, Bhati L, Pandey S, Pandey P, et al. Drug delivery systems: An updated review. International Journal of Pharmaceutical Investigation. 2012; 2(1):2-11. [DOI:10.4103/2230-973X.96920] [PMID] [PMCID]
Fang JY, Hong CT, Chiu WT, Wang YY. Effect of liposomes and niosomes on skin permeation of enoxacin. International Journal of Pharmaceutics. 2001; 219(1-2):61-72. [DOI:10.1016/S0378-5173(01)00627-5]
Mujoriya RZ, Bodla RB. Design and development of niosomal delivery system for ketoprofen. Advances in Life Science and Technology. 2012; 3:1-13. https://www.iiste.org/Journals/index.php/ALST/article/view/963
Srinivas S, Anand Kumar Y, Hemanth A, Anitha M. Preparation and evaluation of niosomes containing aceclofenac. Digest Journal of Nanomaterials and Biostructures. 2010; 5(1):249-54. http://www.chalcogen.ro/249_Srinivas.pdf
Askari M, Nikoonahad Lotfabadi N. [Evaluation of niosomal nano-carriers capabilities on toxicity preservation and delivery of pomegranate peel extract in cell culture conditions (MCF-7 cell line of breast cancer) (Persian)]. Daneshvar Medicine: Basic and Clinical Research Journal. 2018; 26(5):9-20. http://daneshvarmed.shahed.ac.ir/article-1-2015-en.html
Karimi-Moghddam A, Nikoonahad Lotfabadi N, Haghiralsadat BF, Majdizadeh M. [Investigating the effect of lipid nanoparticles containing silibinin anticancer drug on the growth of breast cancer MCF-7 cell line (Persian)]. Journal of Torbat Heydariyeh University of Medical Sciences. 2018; 6(4):1-12. http://jms.thums.ac.ir/article-1-563-en.pdf
Bahrami-Banan F, Sheikhha MH, Ghasemi N, Majdizadeh M, Haghiralsadat BF. [Preparation and study of nano-niosomes containing doxorubicin and evaluation of its toxicity on acute myeloblastic leukemia cell line KG-1 (Persian)]. Journal of Payavard Salamat. 2018; 12(4):309-23. http://payavard.tums.ac.ir/article-1-6592-en.html
Pardakhty A, Shakibaie M, Daneshvar H, Khamesipour A, Mohammadi-Khorsand T, Forootanfar H. Preparation and evaluation of niosomes containing autoclaved Leishmania major : A preliminary study. Journal of Microencapsulation. 2012; 29(3):219-24. [DOI:10.3109/02652048.2011.642016] [PMID]
نوع مطالعه: پژوهشی |
موضوع مقاله:
علوم پايه پزشكي
دریافت: 1398/3/18 | پذیرش: 1398/8/22 | انتشار: 1399/4/1
دریافت: 1398/3/18 | پذیرش: 1398/8/22 | انتشار: 1399/4/1
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |